
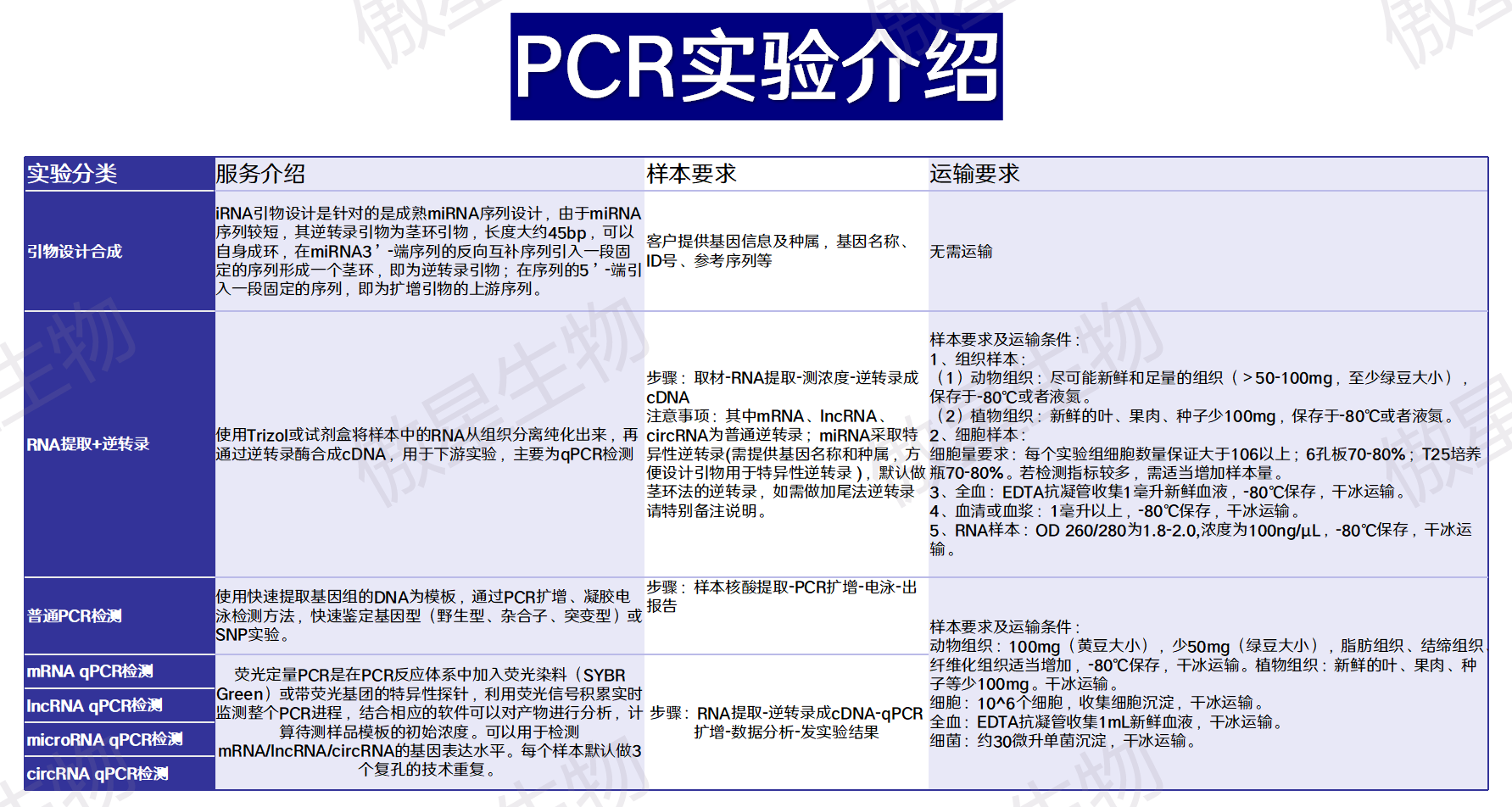
PCR实验介绍
实验步骤
1. 取适量待测样本加入液氮后研磨粉碎;
2. 用1ml Trizol将研磨样本转移到取到1.5ml EP管中;
3. 向1.5ml EP管中加入500ul酚氯,仿振荡混匀后,静止5分钟;
4. 4℃ 12000rpm离心10分钟,小心吸取上清于一新的1.5ml EP管中;
5. 向分离出的上清中加入700ul异丙醇,充分混匀;
6. 4℃ 12000rpm离心10分钟,小心弃上清;
7. 用75%乙醇洗涤沉淀一次,室温晾干;
8. 50ul DEPC水溶解RNA沉淀;
9. 琼脂糖凝胶电泳检测。
使用核酸浓度测定仪测定RNA浓度和纯度,测量前先用溶解RNA用的DEPC水调零,操作方法如下:
1. 抬起样品臂,把样品加到检测基座上;
2. 放下样本臂,使用电脑上的软件开始吸光值检测。在上下两个光纤之间会自动拉出一个样品柱,然后进行检测;
3. 当检测完成后,抬起样品臂,并用干净的无尘纸把上下基座上的样品擦拭干净。
浓度测定
260nm处读值为1表示40 ng RNA/µl。样品RNA浓度计算公式为:A260 X 40 ng/µl。
纯度检测
RNA溶液的A260/A280的比值是一种RNA纯度检测方法,比值范围1.8到2.1。即使比值超出这个范围,RNA样品也一样可以用于一些普通实验中如Northern杂交,RT-PCR和RNA酶保护实验。
逆转录使用invitrogen的逆转录试剂盒superscript III
1. 反应体系1建立:
| RNA | 200ng(10uL) |
| Oligo-dT | 1uL |
2. 混匀,离心。65℃,5分钟,结束后置于冰上。
3. 反应体系2建立:
| 反应体系1 | 12uL |
| dNTP(10uM) | 1uL |
| 0.1M DTT | 2uL |
| 5X Buffer | 4uL |
| RT酶 | 1uL |
4. 混匀,离心。置于42℃,水浴60分钟。
5. 取出后置于85℃,反应10分钟,灭活逆转录酶。
6. 反应结束后将产物置于-20℃待用。
1. Real time PCR反应体系建立:
| cDNA | 2uL |
| PCR mix | 10uL |
| primer F | 1uL |
| primer R | 1uL |
| ddH2O | 6uL |
2. 体系混匀后,瞬离一下,置于荧光定量PCR仪上,按照以下条件反应:
3. Realtime PCR反应条件
| 步骤 | 温度 | 时间 | 循环数 |
| 预变性 | 95℃ | 5 min | 1 |
| 变性 | 95℃ | 10 sec | 40 |
| 退火 | 58℃ | 20 sec | |
| 延伸 | 72℃ | 20 sec | |
| 熔解曲线 | 95℃ | 15 sec | 1 |
| 60℃ | 60 sec | ||
| 95℃ | 15 sec |
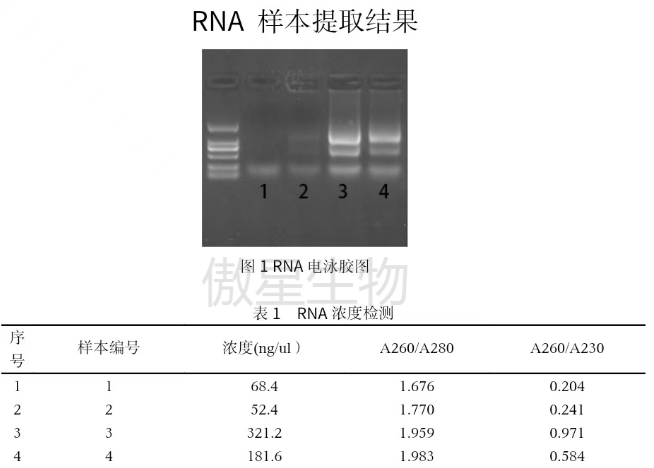
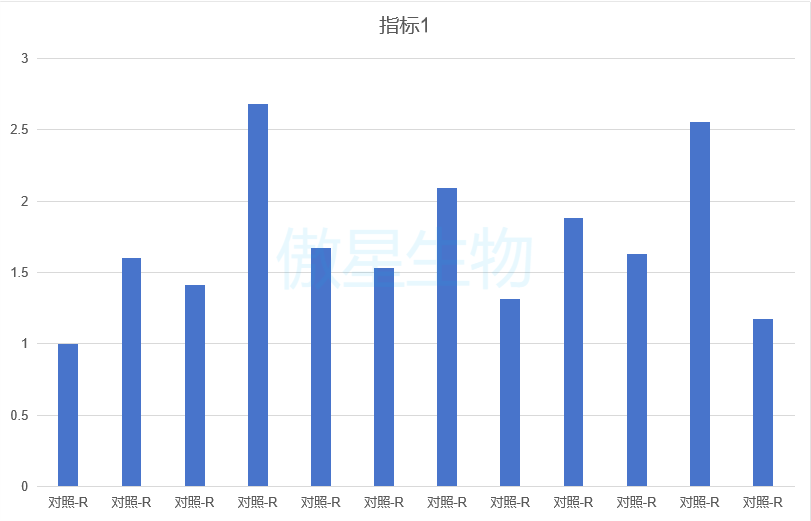
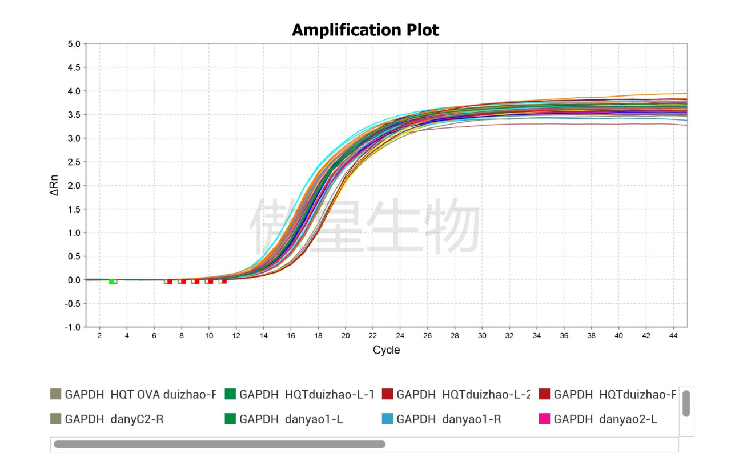
结果示例:
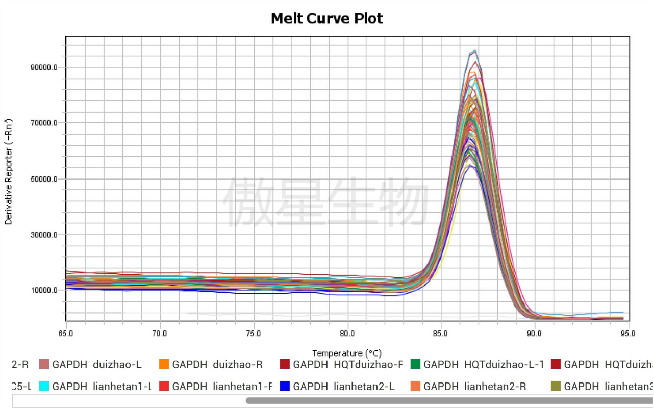
合作流程:
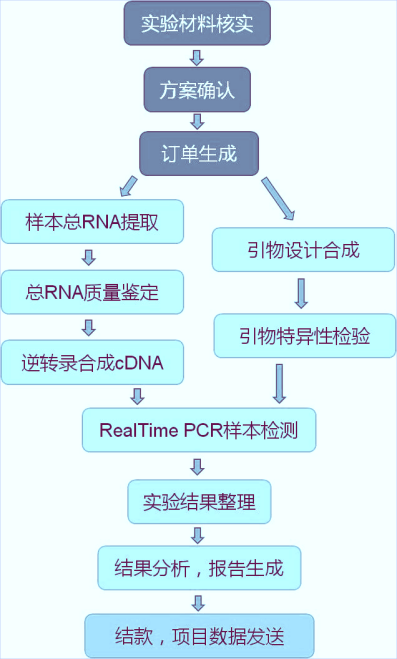
:

科研服务咨询

公众号二维码