
透射电镜概念:透射电镜(Transmission Electron Microscope,TEM),全称透射电子显微镜,是把经加速和聚集的电子束投射到超薄切片的样品上(通常70-90nm),电子与样品中的原子碰撞而改变方向,从而产生立体角散射。散射角的大小与样品的密度、厚度相关,因此可以形成明暗不同的影像,影像将在放大、聚焦后在成像器件上显示出来。是一种高分辨率(0.1nm-0.2nm)、高放大倍数(0.2K-600K)的显微镜。能够清楚的观察到在普通光学显微镜下无法看清的动植物细胞内的超微结构,比如线粒体、内质网、高尔基体、溶酶体、自噬小体、凋亡小体、叶绿体、液泡、细胞内细菌或病毒侵染等结构及病理变化。透射电镜超薄切片除了能够显示细胞内的超微结构之外,还可用于观察病原微生物,如各类细菌真菌等。
扫描电镜概念:扫描电镜(SEM)是一种利用电子束扫描样品表面并收集样品发出的物理信号来获取表面形貌信息的显微技术。扫描电镜的高分辨率和深度信息使其成为一种重要的研究工具,能够提供关于样品表面的详细信息,对于理解和分析材料的性质、生物样本的微观结构以及地质样本的矿物组成等方面具有不可替代的作用。
1、三维形貌的观察和分析。
2、观察形貌的同时,进行微区的成分分析。
透射电镜取材注意事项
样品的取材与固定是生物电镜技术中最关键的一步,样品的质量直接决定了电镜数据的质量。取材导致的结构差,后期实验中无法补救。对取材的基本要求是:确保样品尽可能接近自然生活状态,同时确保位置准确。不同的样品,取材细节上有较大区别,有任何疑问,欢迎咨询联系相关技术人员!
需要的器材:2.5%电镜专用戊二醛、PBS或生理盐水、锋利的手术刀、镊子、牙签、吸管、封口膜、细胞刮、离心机、切割板(光盘或塑料盘)、0℃碎冰(不要冰袋)、1.5ml尖头ep管、铅笔、记号笔。
一、动物组织取材流程及要求
取材流程:(1-3min之内取材完毕)
1、试剂、容器、器械4℃预冷,取材冰上操作(0℃碎冰,不要冻存的冰袋,无条件可室温)。提前滴一些2.5%戊二醛在切割板上;
2、动物麻醉/处死,快速打开需要取材的位置。趁血液还在流动时,迅速切取一块组织,生理盐水或PBS快速冲洗后浸泡到切割板上的戊二醛中进一步切割;
有方向性的样品:如肌丝、脊髓、肠道、血管等,沿着组织伸展方向切成1mm*1mm*3mm的长条,以便分辨方向。
薄片状样品:如视网膜、粘膜等可以切的大一些3mm*3mm左右。
无方向性的样品:选择位置准确的部位切成1mm³小块,切记宁缺毋滥,保证取的每一块都是准确的。如:观察肾小球取肾皮质,观察肺泡避开气管取肺叶。
有被膜的样品:去除被膜或者将被膜破孔方便渗透。样品大小尽量接近,不规则或稍大一点没关系。一定要避免修整样品时造成边缘组织机械损伤,这样反而效果不好。
3、切的时候避免刀片对样品的挤压,应该拉刀法(斜着前后拉动手术刀)切断,切样时,配合牙签轻轻拨动样品,将样品切成符合要求的形状。疏松多孔及柔软的样品可以大一些,避免样品溶解或压坏。最后将样品用沾水的牙签粘入1.5ml尖头EP管。不要用镊子夹样品。加满2.5%戊二醛。4℃避光保存。如果样品漂浮,可用纸或纱布将组织压到液面以下。
4、取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
注意事项:
1、组间位置一致。同一器官不同部位的同种细胞,结构也有较大差异;
2、器具锋利,柔软的组织要用手术刀轻轻拉断,尽量避免压断,保证切面锋利。
3、冰上操作时,用制冰机的碎冰,如果没有碎冰,可以室温取材,冰袋易冻伤样品。
4、取材速度,条件是灵活的,把握整体原理,不要刻意为了保证位置或大小,切坏了样品。尤其是要避免样品挤压以及冰袋冻坏样品。
关于灌注取材:
灌注取材要求较高,尽量不要灌注。因为灌注不充分,反而会导致超微结构较差。较大且较深,不好定位的组织,可以选择灌注。要求如下:
1、灌注液建议:终浓度为4%多聚甲醛+1%戊二醛混合液,稀释液为PB(配方参考附件);
2、多聚甲醛和戊二醛均为电镜专用,多聚甲醛建议新鲜配置7天以内的;
3、灌注方式以机械泵辅助灌注,尽量灌注充分。灌注不充分会导致部分区域结构差。
4、灌注完成之后,按上述要求电镜取材,样品固定在2.5%戊二醛中,4度邮寄给我们。较大且较深的组织,振动切片成150-200um的厚片固定,方便后续操作。
二、细胞细菌取材流程及要求
贴壁细胞取材流程:细胞取材有2种方法,分别为刮取法和消化法。均有各自的优缺点,请根据情况酌情取材。
| 取材方法 | 优点 | 缺点 |
| 刮取法(推荐) | 1、保持了细胞最原始结构;2、细胞损伤较小,最大程度还原了样品真实结构,实验室会挑选完整细胞拍摄; | 1、细胞切面多呈长条形或梭形;2、胞浆视野会稍窄一些; |
| 消化法 | 细胞呈饱满圆形,胞浆视野广 | 1、细胞会有损伤,线粒体空泡化严重、内质网扩张、自噬假阳性等;2、细胞间结构破坏。无法观察细胞间结构。如:紧密连接。 |
刮取法操作流程:
1、请用6cm-10cm的培养皿培养细胞,方便后续操作;
2、细胞倒掉培养液,加入恢复至室温的戊二醛固定液2ml。
3、细胞常温避光固定5min后,用细胞刮刀斜45°朝一个方向快速铲下,保持一个方向,不要来回刮;
1、得到的细胞悬液吸入离心管,离心(1500-3000rpm)3-5min,弃上清,然后加入新的电镜固定液。再次更换固定液后,室温避光固定30min后,4℃保存。细胞团块需要有绿豆大小,如图所示。太大的团块建议吹散重悬。
5、取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
消化法特点操作流程:
1、培养好的细胞(细胞密度不超过70%)弃培养基,加入胰酶消化。
2、胰酶消化好后(时间不宜过长),加培养基终止消化,吸管轻轻吹打至细胞起浮。吸入离心管,低速离心(1500-3000rpm),3-5min左右,细胞团要有绿豆大小,如图所示。
3、弃上清,加入电镜固定液(室温),细胞量多需要吹散,少量细胞无需吹散。
4、室温避光固定30min,再转移至4°保存运输。
5、取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
悬浮细胞取材流程:
细胞悬液离心(1500-3000rpm)3-5min,弃掉培养基后加入2.5%戊二醛室温避光固定30min,再转入4℃保存,4℃冰袋运输。细胞团块需要有绿豆大小,如图所示。太大的团块可用牙签挑成几块。取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
细菌取材流程:
1、固定培养的细菌:牙签挑取菌落置于室温2.5%戊二醛,避光固定30min。再转入4℃保存,4℃冰袋运输。样品包裹厚一点,不要和冰袋直接接触,以免冻伤。细胞团块需要有绿豆大小,如图所示。太大的团块可用牙签挑成几块。
2、悬浮细菌:细菌悬液离心(5000-10000rpm)3-5min,弃掉培养基后加入2.5%戊二醛室温避光固定30min,再转入4℃保存。细胞团块需要有绿豆大小,如图所示。4℃冰袋运输。取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
注意事项:
1、不要反复来回刮细胞,会造成细胞大量损伤;
2、离心的目的是让细胞聚集成团,转速不可太高,会导致细胞变形;
3、样品保存邮寄时,避免冻伤。
三、外泌体、噬菌体、病毒、脂质体等:
1、建议提供浓缩液至少50ul,样品的纯度及浓度尽量高。
2、保存及运输方式以样品结构性状稳定为要点。如:冻存的外泌体及病毒,不好反复冻融,所以建议干冰邮寄。新鲜提取的外泌体及噬菌体等,4℃可存放3-5天,所以样品可冰袋邮寄。部分样品可能在常温更能稳定保存其形态,即可常温邮寄。
3、取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。
四、植物组织取材及要求
取材流程:
1、PBS冲洗样品表面,去除泥沙等污染物。
2、用锋利的手术刀或剪刀切割样品,切样时,可配合牙签轻轻拨动样品,将样品切成符合要求的形状,有方向的样品:如根尖、茎等,沿着组织伸展方向切成1mm*1mm*3mm的长条,以便分辨方向。薄片状样品可以切的大一些3mm*3mm左右。没有方向的样品切成1mm³小块,切记宁缺毋滥,保证取的每一块都是准确的,如观察果皮就要去除果肉。观察果肉就要去除果皮。观察叶片就需要避开叶脉。有膜壳的样品要去除膜壳或者将膜壳破孔方便渗透;
2、注意切割边缘整齐,去除机械损伤的位置。
3、最后将样品用沾水的牙签沾入1.5ml尖头EP管。加满2.5%戊二醛。4℃避光保存。不要用镊子夹样品。如果样品漂浮,可用纸或纱布将组织压到液面以下。如果需要抽气,注意抽气的程度,太强烈可能会导致结构变化。
4、取好的样品封口膜封口,气泡膜包裹厚一点再邮寄。样品不要和冰袋直接接触,防冻伤。
注意事项:
1、组间位置一致。同一器官不同部位的同种细胞,结构也有较大差异;
2、样品大小尽量接近,不规则或稍大一点没关系。
3、器具锋利,柔软的组织要用手术刀轻轻拉断,尽量避免压断,保证切面锋利。一定要避免修整样品时造成边缘组织机械损伤,这样反而效果不好。
4、冰上操作时,用制冰机的碎冰,如果没有碎冰,可以室温取材,冰袋易冻伤样品。
5、取材速度,条件是灵活的,把握整体原理,不要刻意为了保证位置或大小,切坏了样品。尤其是样品挤压以及冰袋冻坏样品。
五、样本储存运输标准
储存:样本取材后,4℃避光保存时间最好不超过1个月。
运输:固定液充满EP管,封口膜封口。如下图,气泡膜或报纸包裹7-8层。纸质送样单+泡沫盒+冰袋的方式运输,冰袋2-3个(-20℃冰袋,不要太多,夏季3-4个),顺丰寄付。
附件:戊二醛配方
1、0.2M 磷酸缓冲液配方:
A液:0.2mol/L磷酸二氢钠水溶液:
NaH2PO4.H2O27.6g 或 NaH2PO4.2H2O 31.21g加双蒸水到1000ml
B液:0.2mol/L磷酸氢二钠水溶液:
Na2HPO4.2H2O 35.61g 或 Na2HPO4.12H2O 71.64g加双蒸水到1000ml
A液23ml+B液77ml混合得到0.2M磷酸缓冲液。
2、2.5﹪戊二醛固定液配方:
0.2M磷酸缓冲液50ml+25﹪戊二醛(电镜专用)10ml+双蒸水,定容至100ml
调整pH 值 7.3-7.4
六、结果示例:
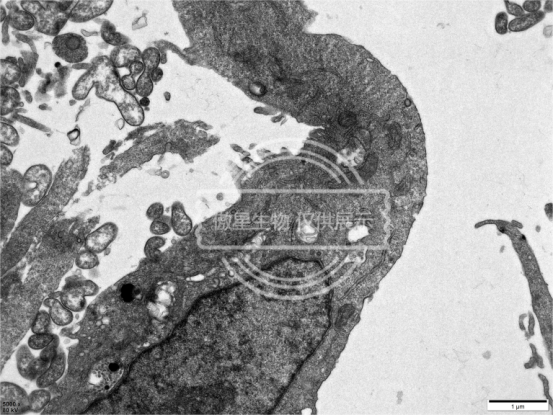
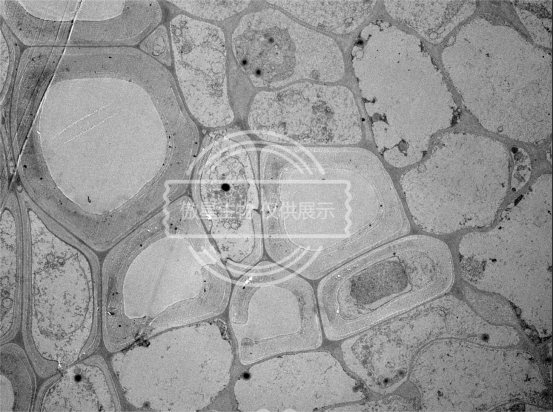
扫描电镜取材注意事项
一、细胞爬片、盖玻片等培养的细胞样品:
推荐用六孔板或培养皿培养细胞爬片样品,弃掉培养基, PBS 快速洗 2 遍, 弃掉 PBS,加入2.5%电镜专用戊二醛固定液固定。固定液可以多加一些, 样品需要完全浸没在固定液里, 4 ℃固定 12h 以上。加满2.5%戊二醛固定液, 样品封口膜封口, 气泡膜包裹, 然后泡沫盒+ 冰袋快递运输。
二、固体培养基培养的细菌样品:
已经长成菌落的细菌样品,直接用棉签或者牙签挑起米粒大小菌落,转入 2.5%戊二醛固定液中, 1.5ml的ep 管,固定液加满,4 ℃固定 12h 以上。泡沫盒+冰袋快递运输。
三、悬浮细胞、菌液、藻液等样品:
样品离心, 弃上清, PBS 洗 2 次,弃 PBS,加入 2.5%戊二醛固定液,转入1.5m的ep 管, 加满2.5%戊二醛固定液,样品封口膜封口, 气泡膜包裹, 4 ℃固定 12h 以上,泡沫盒+冰袋快 递运输。对于细菌样品, 如果需要观测鞭毛, 请尽量让细菌自然沉淀, 去除上清时尽量操作轻柔,离心会使鞭毛脱落。
四、动植物植物组织样品:
动物组织: 动物麻醉, 处死,快速切取需要观察的组织部位, 生理盐水冲洗血液,用锋利的剪刀或手术刀暴露出需要观察的面。管状组织切成0.5cm长度的小段,其他无方向性的组织切成0.5cm*0.5cm*0.5cm左右的小块。请注意切取的小块必须包含待测结构且方便辨认, 特别是对于有方向性的样品,注意区分方向。取材后于2.5%戊二醛4℃固定保存12h以上, 邮寄时固定液加满, 样品封口膜封口,气泡膜包裹,泡沫盒+冰袋快递运输。
植物组织: 植物样品用PBS或者蒸馏水冲洗,去除表面环境杂质,然后用锋利的手术刀或剪刀切取需要观察的部位, 叶片切成: 0.5cm*0.5cm大小,根切取0.5cm左右长度的小段。其他果实或组织0.5cm*0.5cm*0.5cm左右。请注意切取的小块必须包含待测结构且方便辨认, 特别是对于有方向性的样品,注意区分方向。取材后于2.5%戊二醛4℃保存,如果样品漂浮, 需要用真空泵反复抽沉, 或者用棉花或纱布将样品压到液面以下。 4℃保存12h以上。对于邮寄时固定液加满, 样品封口膜封口,气泡膜包裹,泡沫盒+冰袋快递运输。
五、干燥样品:
对于干燥的种子、材料等样品, 可直接邮寄, 无需固定。
样品保存及邮寄:
1、储存:样本取材后,4℃保存时间尽量不超过1个月。
2、运输:固定液充满EP管,封口膜封口,气泡膜或报纸包裹厚一些。最后泡沫盒+冰袋的方式运输, 冰袋2-3个(-20℃冰袋,不要太多) ,一定要与样品隔开。特殊样品如脂肪、 植物等,用纱布将样品压到液面以下,保证充分固定。
扫描电镜结果示例:
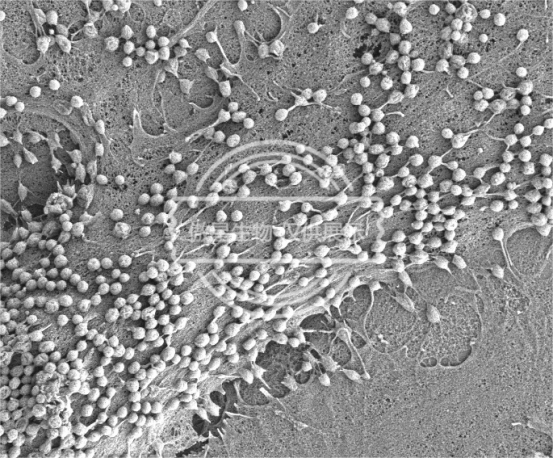
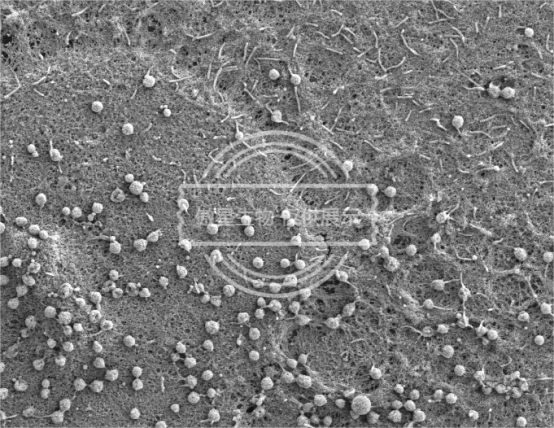

科研服务咨询

公众号二维码