
免疫荧光技术(immunofluorescence technique)是在免疫学、生物化学与显微镜技术的基础上建立起来的一项技术。用荧光抗体示踪或检查相应抗原的方法称为荧光抗体法;用已知的荧光抗原标记物示踪或检查相应抗体的方法,称为荧光抗原法。这两种方法总称为免疫荧光技术。但实际工作中荧光抗原技术应用很少,所以常将荧光抗体技术称为免疫荧光技术。
荧光单标:
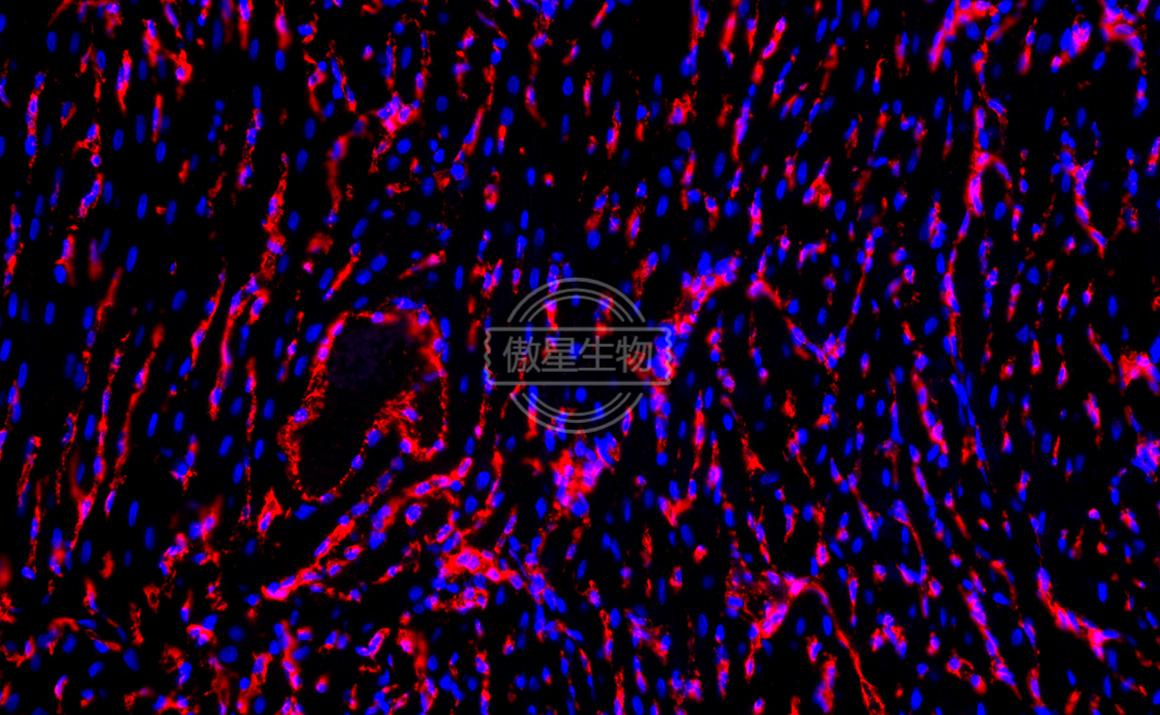
在一张切片上对一个抗原进行标记,即为免疫荧光IF单标,可直接在组织切片、细胞涂片或培养细胞爬片上原位显示某些蛋白质或多肽类物质,通常可标记红光或绿光,细胞核用DAPI标记。
荧光双标:
在一张切片上对两个抗原进行标记,即为免疫荧光IF双标,可直接在组织切片、细胞涂片或培养细胞爬片上原位显示某些蛋白质或多肽类物质,普通方法免疫荧光双标要求一抗来源不能相同,若是相同,二抗无法区分。不同的一抗对应标记不同颜色,可以用于定位两种不同的抗原。
荧光三标:
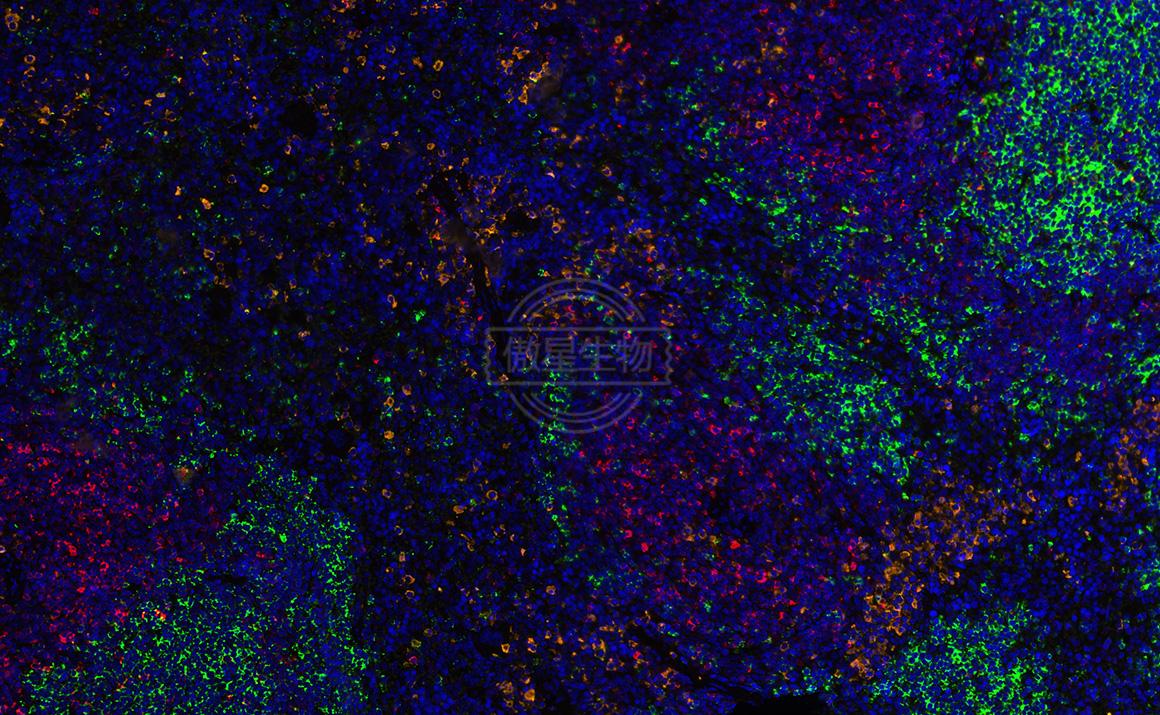
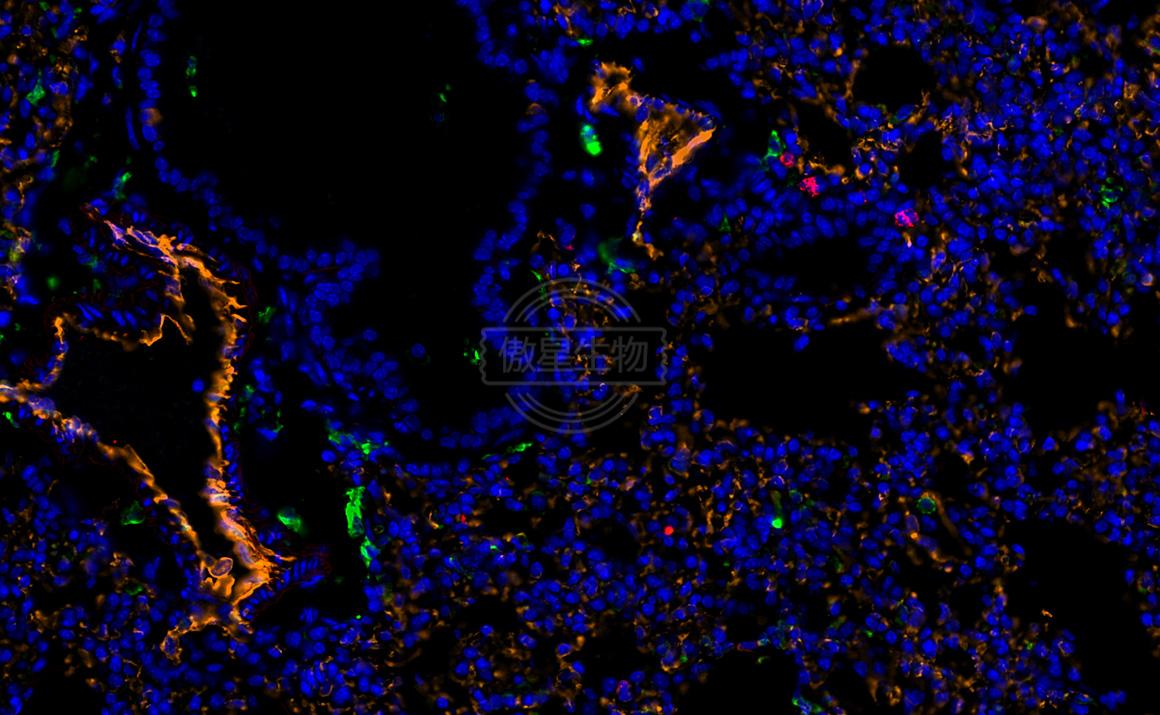
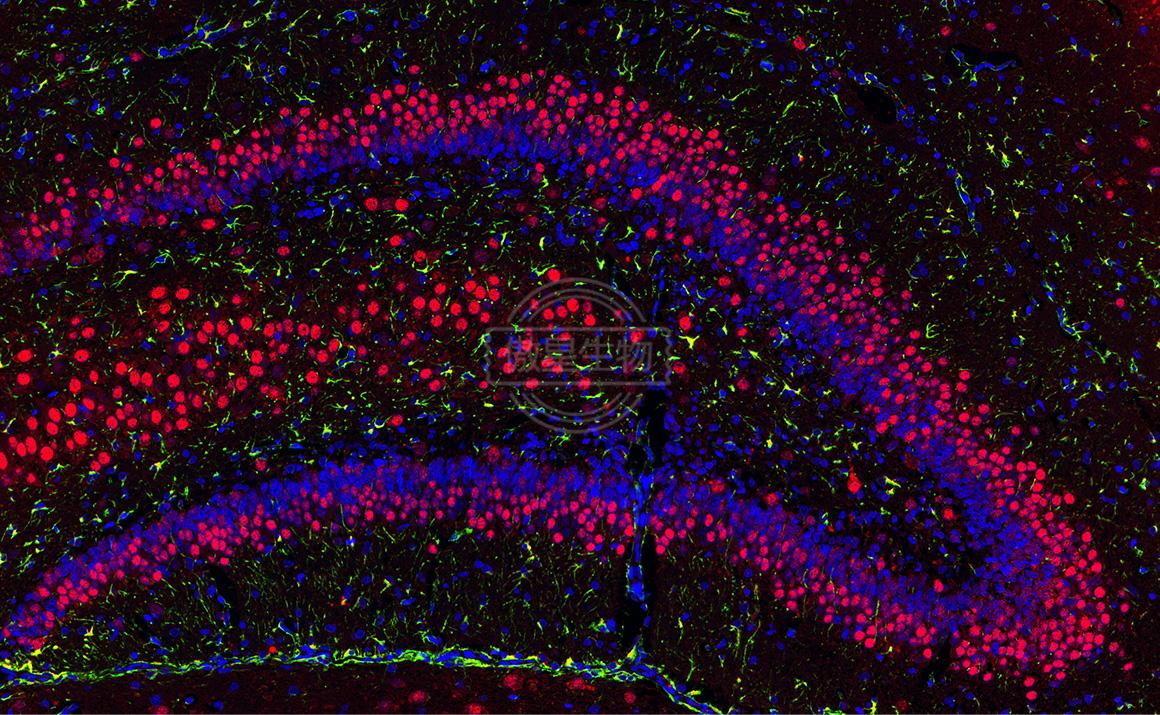
在一张切片上对三个抗原进行标记,即为免疫荧光IF三标,可直接在组织切片、细胞涂片或培养细胞爬片上原位显示某些蛋白质或多肽类物质,普通方法免疫荧光三标要求一抗来源不能相同,若是相同,二抗无法区分。不同的一抗对应标记不同颜色,可以用于定位三种不同的抗原。
免疫荧光染色及成像分析是研究组织形态和组织原位抗原表达不可或缺的检测技术,广泛应用于临床病理和医学及生物学研究的各个领域。凡是可以作为抗原或半抗原的物质,如:蛋白质、多肽、氨基酸、多糖、磷脂、酶、激素、病原体及受体等,都可以在细胞、亚细胞水平检测到。
免疫荧光技术根据抗原抗体特异性结合的原理,先将已知抗体(或抗原)标记上荧光基团,再利用这种荧光抗体(或抗原)作为探针来检测固定细胞或组织内的相应抗原(或抗体)。在荧光显微镜下观察,当抗原抗体复合物中的荧光素受激发光照射后,会发射出一定波长的荧光,从而确定靶抗原(或抗体)的性质与定位,还可利用定量技术(如:流式细胞仪)测定含量。
脱蜡与水化-抗原修复-血清封闭-孵育一抗-孵育二抗-DAPI染核-封片-显微镜镜检。
1、提供固定合格的样本。组织离体后,选择合适的固定液立即固定,固定液的量建议大于组织体积的10-15倍,新鲜标本用合适的容器固定24-48h,大标本固定12h,再切开固定。标本常温(24℃左右)或冷藏(4℃)固定,切勿冷冻结冰,固定样本常温运输送样。
2、涂片和爬片必须充分固定,石蜡切片实验前需充分脱蜡。
3、提供准确的抗体信息。
结果示例:

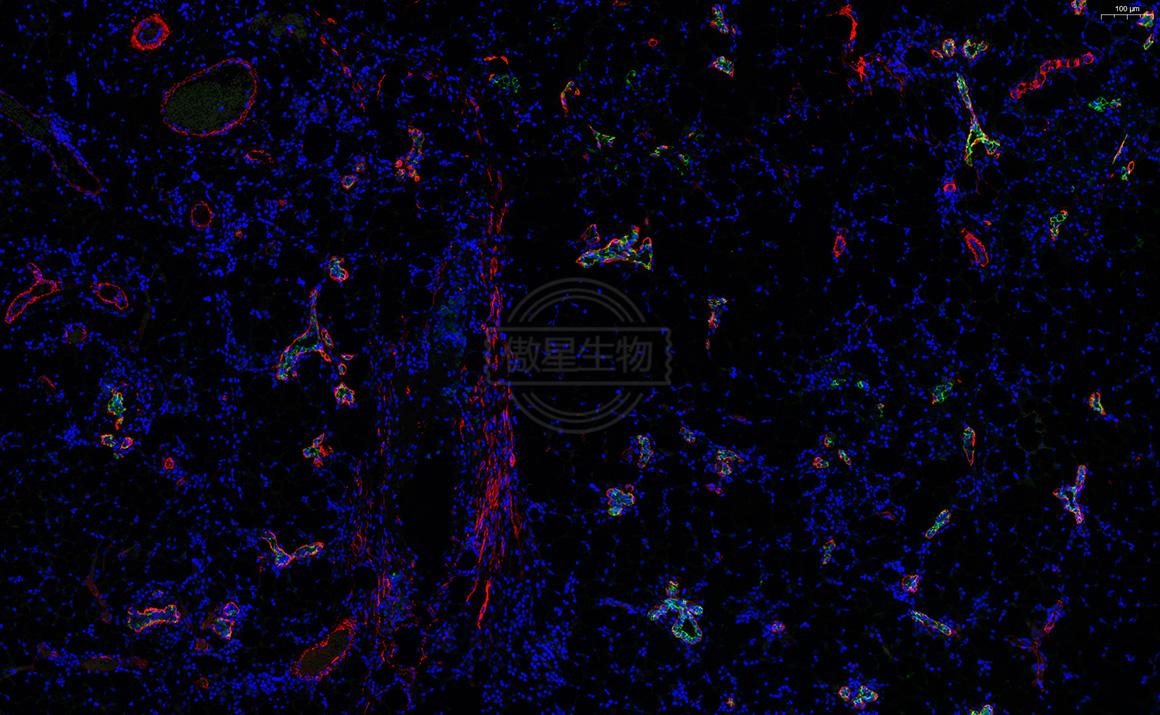
实验常见问题解答:
1、为什么背景染色较深?
1)抗体浓度过高:一抗浓度过高是常见的原因之一。解决办法是,每次使用新抗体前应当对其工作浓度进行测试,使每一抗体个体化,找到适合自己实验室的理想工作浓度,既使是即用型的抗体也应如此,不能只简单的按说明书进行染色。
2)抗体孵育时间过长或温度较高:解决办法是,严格执行操作规程,更好随身佩带报时表或报时钟,及时提醒,避免因遗忘而造成时间延长。现在流行的二步法(Polymer)敏感性很高,要求一抗孵育的时间不是传统的1小时,而是30分钟,因此,要根据染色结果进行调整。
3)DAB变质和显色时间太长:DAB更好现用现配,如有沉渣应进行过滤后再用。配制好的DAB不应存放时间太长,因为在没有酶的情况下,过氧化氢也会游离出氧原子与DAB产生反应而降低DAB的效力,未用完的DAB存放在冰箱里几天后再用这种似乎节约的办法是不可取的。DAB的显色更好在显微镜下监控,达到理想的染色程度时立即终止反应。不过当染色片太多时或用染色机时,这样做似乎不现实,但至少应对一些新的或少用的抗体显色时进行监控,避免显色时间过长。
4)组织变干:修复液溢出后未及时补充液体、染色切片太多、动作太慢、忘记滴液、滴液流失等都是造成组织变干的原因。解决的办法是操作要认真仔细,采用DAKO笔或PAPPen在组织周围画圈,可以有效的避免液体流失,也能提高操作速度。
5)切片在缓冲液或修复液中浸泡时间太长(大于24小时):原因上不清楚,但现象存在。有的实验室喜欢前将切片脱蜡至修复,第二天加抗体进行免疫组化染色,如果将装有切片和修复液的容器放在4ºC冰箱过夜,对结果无明显影响,如果放在室温,特别是炎热的夏天,会出现背景着色,因此,不可存放时间太长。
6)一抗变质、质量差的多克隆抗体:注意抗体的有效期,过期的抗体要么不显色要么背景着色。用新买抗体时更好设立阳性对照和用使用过的抗体作比较。
2、为什么定位不准确?
1)细胞核干扰:细胞核位置前面的细胞质染色干扰造成,可以降低抗体浓度,孵育时间
2)细胞或者组织状态不对:细胞或者组织状态不同导致你的目的蛋白细胞定位不同,造成最后的定位不对,如果一直出现定位不对问题,建议重新培养细胞调整好状态或者重新取材,进行再次染色。
3)共定位问题解析:假设想证明某一细胞发生某种变化,换句话说就是既有某种蛋白表达,又有另一种蛋白表达,两种蛋白属于共定位,该种情况可以采用免疫双标记检测;如果两种蛋白不属于共定位,假设一种在膜上表达,一种在胞浆表达,该种情况应该不属于共定位,属于共表达,这时候实验应该重新设计去验证你的结论。
4)核定位不对:核内表达的抗原定位用免疫荧光或者免疫酶标都可以。如果定位不正确,建议封闭和打孔合为一步,即在封闭液中添加0.5% TRITON-100,37度封闭2小时,加一抗后最好4度孵育过夜(16小时)。

科研服务咨询

公众号二维码