
用标记的特异性抗体,对组织切片或细胞标本中某些化学成分的分布和含量,进行组织和细胞原位定性、定位或定量研究,这种技术称为免疫组织化学(immunohistochemistry)技术或免疫细胞化学(immunocytochemistry)技术。
本实验是将组织细胞内的抗原可视化过程,可直接在组织切片、细胞涂片或培养细胞爬片上原位显示某些蛋白质或多肽类物质,并可精确到亚细胞结构水平。载玻片上的组织细胞经过预处理(脱蜡至水、抗原修复等)后,孵育相应的抗体,此时抗原(多肽、蛋白质、外源性物质等)被第一抗体特异性识别结合,然后把第一抗体作为抗原继续通过第二抗体特异性识别结合(第二抗体上有标记特定物质),若第二抗体标记的特定物质为辣根过氧化物酶(HRP),可与DAB在特定条件下反应形成棕褐色沉淀,最后通过显微镜观察。
免疫组织化学技术可借助显微镜的显像与放大作用,在细胞、亚细胞水平检测各种抗原物质(如蛋白质、多肽、氨基酸、多糖、磷脂、酶、激素、病原体及受体等)。在病理学中,免疫组化技术常用来进行肿瘤的诊断及鉴别诊断,也可通过此技术对肿瘤进行更细化的分类。
根据抗原抗体反应(即抗原抗体特异性结合)和化学显色原理,引入附有标记物的外源性抗体(或抗原),使之锚定于组织或细胞标本中相应的抗原(或抗体),标记物经呈色反应来显示待检抗原(或抗体)。
脱蜡与水化-抗原修复-灭活内源性过氧化物酶和生物素-血清封闭-孵育一抗-孵育二抗-DAB显色-苏木素复染-脱水与透明-封片-显微镜镜检。
1、提供固定合格的样本。组织离体后,选择合适的固定液立即固定,固定液的量建议大于组织体积的10-15倍,新鲜标本用合适的容器固定24-48h,大标本固定12h,再切开固定。标本常温(24℃左右)或冷藏(4℃)固定,切勿冷冻结冰,固定样本常温运输送样。
2、涂片和爬片必须充分固定,石蜡切片实验前需充分脱蜡。
3、提供准确的抗体信息。
实验结果:
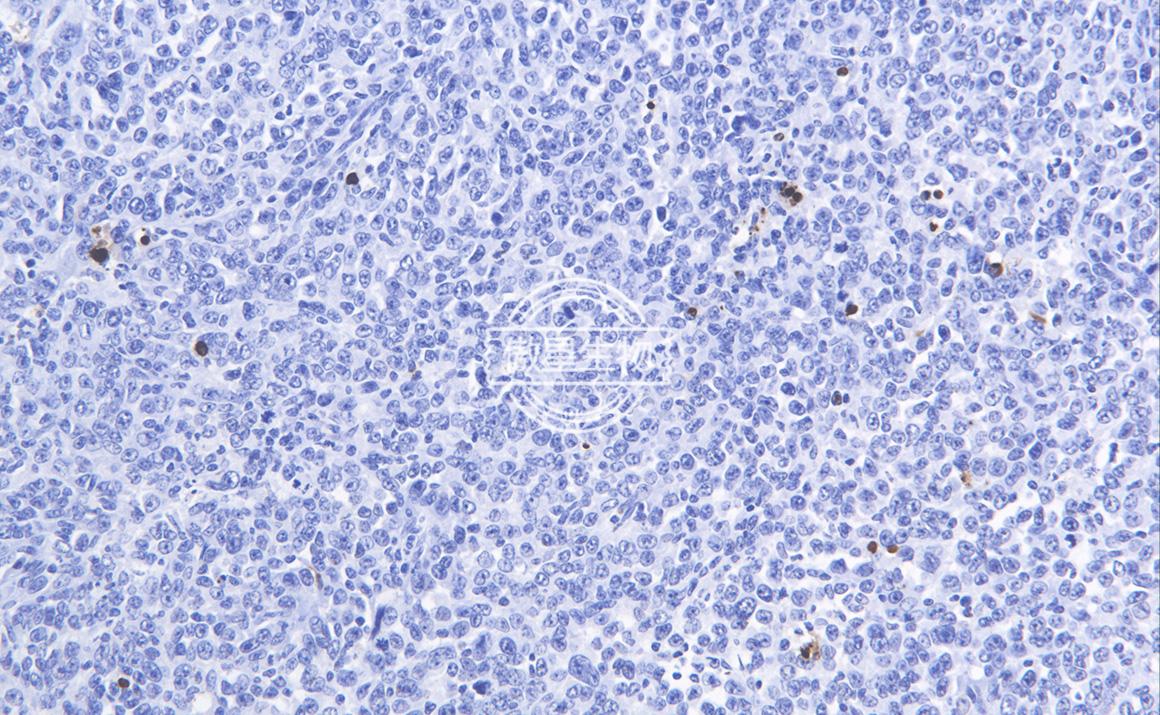
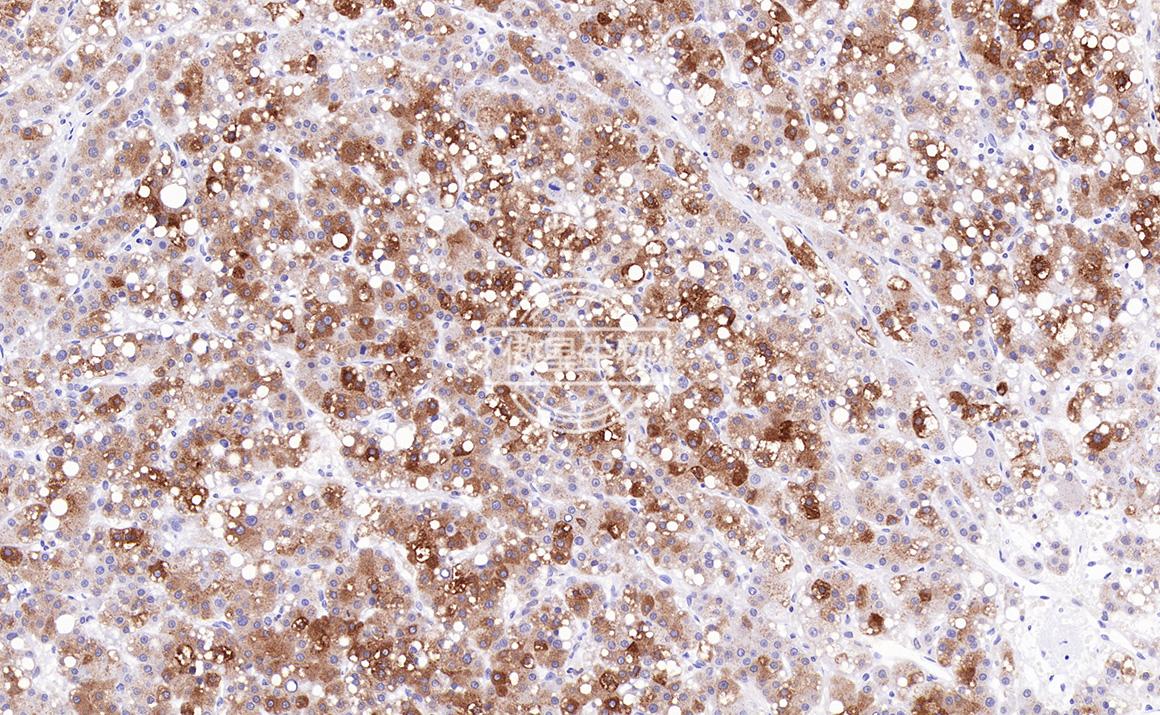
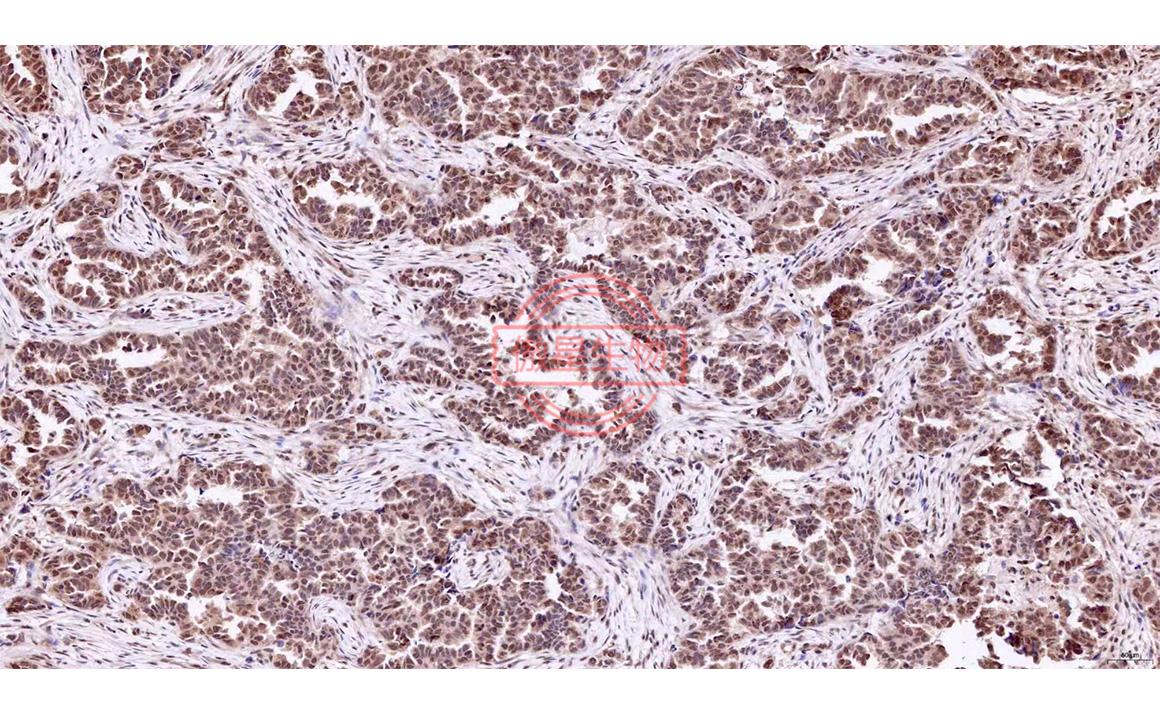
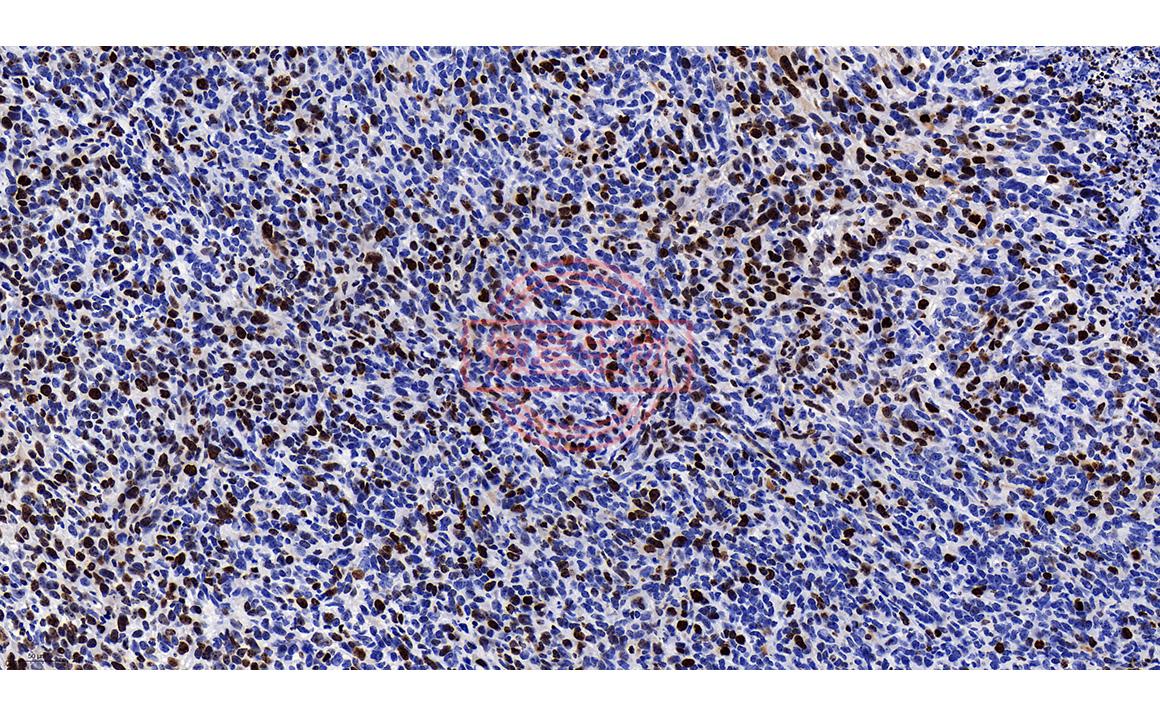
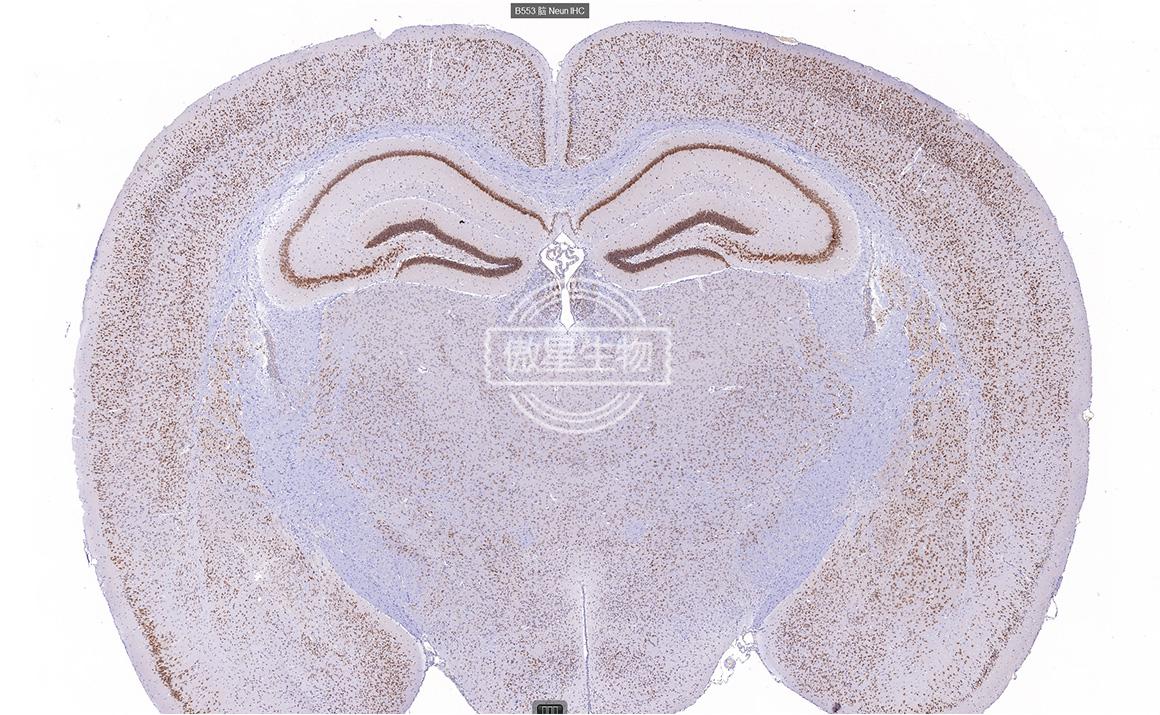
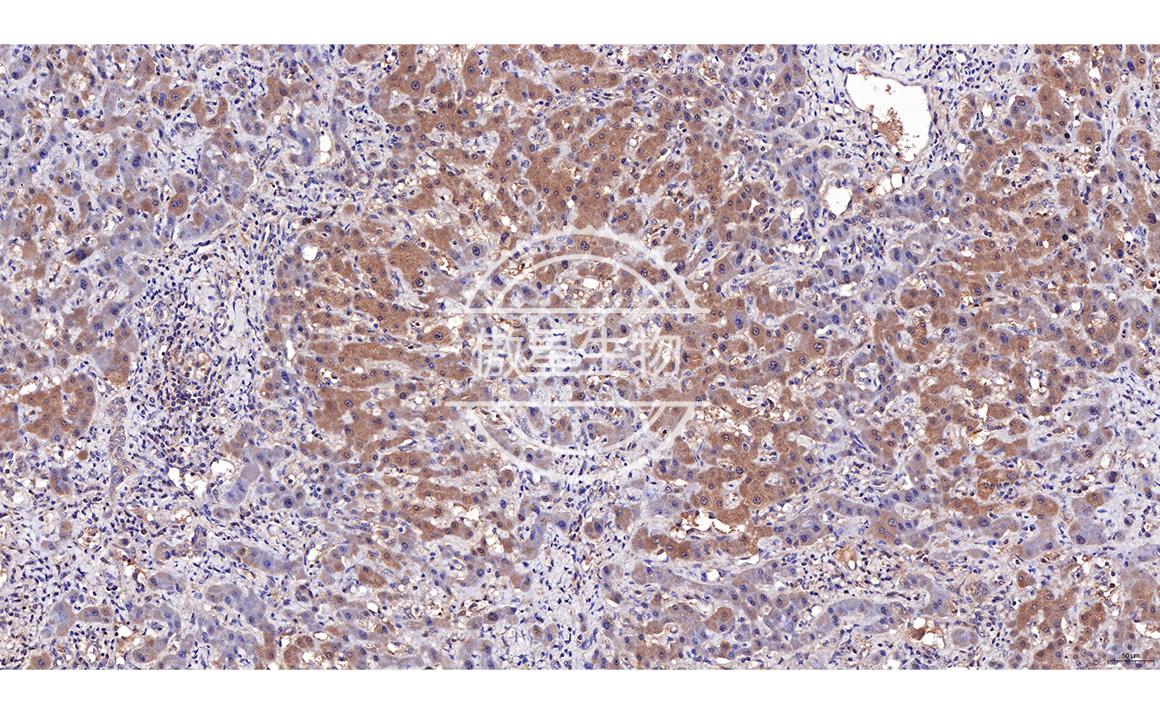
免疫组化常见问题解答:
1)产生组织切片非特异性染色的原因有哪些? 如何解决?
1 、 抗体孵育时间过长、抗体浓度高易增加背景着色。这可通过缩短一抗/二抗孵育时间、稀释抗体来控制。这是 最重要的一条。
2 、 一抗用多克隆抗体易出现非特异性着色,建议试用单克隆抗体看看。
3、内源性过氧化物酶和生物素在肝脏、肾脏等组织含量很高(含血细胞多的组织),需要通过延长灭活时间和增加 灭活剂浓度来降低背景染色;
4 、 非特异性组分与抗体结合,这需要通过延长二抗来源的动物免疫血清封闭时间和适当增加浓度来加强封闭效果;
5 、 DAB 孵育时间过长或浓度过高;
6 、 PBS 冲洗不充分,残留抗体结果增强着色, 在一抗/二抗/SP 孵育后的浸洗尤为重要;
7 、 标本染色过程中经常出现干片,这容易增强非特异性着色。
2)免疫组化染色呈阴性结果的原因有哪些?
1、抗体浓度和质量问题以及抗体来源选择错误。不是抗体浓度越高就越易出现阳性结果,抗原抗体反应有前带和 后带效应, 必须摸索最佳浓度。
2、抗原修复不全,对于甲醛固定的组织必须用充分抗原修复来打开抗原表位,以利于与抗体结合; 建议微波修复 用高火 4 次*6min 试试。有人做过实验,这是最佳的时间和次数。若不行, 还可高压修复。
3、组织切片本身这种抗原含量低。
4 、血清封闭时间过长。
5 、DAB 孵育时间过短。
6 、细胞通透不全, 抗体未能充分进入胞内参与反应。
7、开始做免疫组化,建议一定要首先做个阳性对照片, 排除抗体等问题。
3)石蜡切片和冰冻切片的比较?
1 、要求做冰冻切片的不一定能做石蜡切片。因为做石蜡切片时要高温烤片,可能会破坏组织的抗原性,如果组织 的抗原性较稳定,则可作石蜡切片;但是要求做石蜡切片的,可作冰冻切片。
2 、冰冻切片的优点是能够较好的保存组织的抗原免疫活性,做免疫组化时不需抗原修复这一步。缺点是细胞内易 形成冰晶而破坏细胞结构,可能会使抗原弥散;切片厚度较石蜡的厚,做的片子没石蜡的漂亮。当你买一抗时, 目 录上都写着做什么样的切片, 如果它写着只能做冰冻,就不能做石蜡,如写着两者都可,那就都能做。
3 、石蜡切片的优点可以保持组织细胞的形态结构,且容易存放在室温,而冰冻切片比较麻烦,一定要存在-80 度的 低温冰箱中,尤其是用来做原位杂交的的切片,为了防止 RNA 降解,保存一贯很重要。由于石蜡切片可以切到 4 微米左右, 所以原位杂交探针容易渗透到组织中去,容易成功,而且得到的颜色/形态都较冰冻切片好。
4)如何选择一抗?
1 、单克隆和多克隆抗体的选择。由一种克隆产生的特异性抗体叫做单克隆抗体。单克隆抗体能目标明确地与单一 的特异抗原决定簇结合,就像导弹精确地命中目标一样。另一方面,即使是同一个抗原决定簇,在机体内也可以由 好几种克隆来产生抗体,形成好几种单克隆抗体混杂物,称为多克隆抗体。在抗原抗体反应中,一般单克隆抗体特 异性强,但亲和力相对小,检测抗原灵敏度相对就低; 而多克隆抗体特异性稍弱,但抗体的亲和力强,灵敏度高, 但易出现非特异性染色(可以通过封闭等避免)。
2 、应用范围的选择。有的一抗只能用于 Western blotting,或免疫组化、免疫荧光、免疫沉淀等;甚至标明石蜡切 片或冰冻切片。
3 、种属反应性的选择(species reactivity)。这一点很重要,表明这种抗体可能存在种属差异,且这种抗体适合检测 哪种种属动物体内的抗原。
4 、种属来源,一般兔来源的多是多克隆抗体;而小鼠来源的多是单克隆抗体,但也有另外。根据此来源来选择相 应的二抗。
5 、生产厂家的选择。
5)在什么情况下使用 TritonX-100?
1 、Triton X-100 化学名称为聚乙二醇辛基苯基醚,是一种去污剂。在免疫组织化学(>10um 厚切片) 和免疫细胞化学 中一般用 Triton X-100 作为细胞通透剂,在膜上打孔。
2 、其作用原理: Triton X-100 可以溶解细胞膜、细胞核膜、细胞器膜上的脂质而使抗体及大分子结构的物质进入胞 浆和胞核内,故在细胞免疫组化时尤为推荐使用,这样抗体就能顺利进入胞内与相应抗原结合。
3 、Triton X-100 既是一种表面活性剂,也有抗氧化作用。
6)封闭血清的选择原则是什么?
1 、膜上或切片上有剩余的位点可以非特异性吸附抗体, 造成后续结果的假阳性。
2 、封闭血清一般是和二抗同一来源的,血清中动物自身的抗体, 预先能和组织中有交叉反应的位点发生结合, 否 则在后面的步骤中如果和二抗发生结合,会造成背景。
3 、也可以用小牛血清、 BSA、羊血清等,但不能与一抗来源一致。
7)抗体孵育条件的比较?
1 、一抗孵育温度有几种:4 度、室温、 37 度,其中4 度效果最佳;孵育时间: 这与温度、抗体浓度有关, 一般 37 度 1-2h ,4 度过夜(从冰箱拿出后 37 度复温 45min)。
2 、二抗一般室温或 37 度 30min-1h,具体时间需要摸索。
8)一抗 4 度孵育后为什么要进行 37 度复温?
1 、一方面,防止切片从 4 度直接放入 PBS 易脱片;
2、另一方面,使抗原抗体结合更稳定。一般不需要,但对表达较弱的抗原可能有用,4 度和 37 度时分子运动方式不同, 前者分子碰撞机率和运动速度小于后者,后者结合更快,但敏感性也提高了并易造成非特异染色。
9)DAB 显色时间如何把握?
1 、DAB 显色时间不是固定的,主要由显微镜下控制显色时间, 到出现浅棕色本底时即可冲洗;
2 、DAB 显色时间很短(如几秒或几十秒)就出现很深的棕褐色,这很可能说明你的抗体浓度过高或抗体孵育时间 过长,需要下调抗体浓度或缩短你的抗体孵育时间;
3 、此外,若很短时间就出现背景很深,还有可能你前面的封闭非特异性蛋白不全, 需要延长封闭时间;
4 、DAB 显色时间很长(如超过十几分钟)才出现阳性染色,一方面可能说明你的抗体浓度过低或孵育时间过短(最 好一抗 4 度过夜); 另一方面就是封闭时间过长。
10)免疫组化结果如何分析?
1 、阳性着色细胞计数法。在 40×光镜下,随机选择不重叠的 10 个视野,人工或机器计数阳性着色细胞,每组 3~6 张不同动物组织切片,然后进行组间比较即可。
2 、灰密度分析法。通过在不同组别和不同动物组织切片上选择相同区域、相同条件下用 image j 进行灰密度分析, 然后进行统计分析即可。
3 、评分法。通过在光学显微镜下对组织切片分别按染色程度(0~3 分为阴性着色、淡黄色、浅褐色、深褐色)、阳 性范围进行评分(1~4 分为 0~25% 、26~50% 、51~75% 、76~100%),最终可以分数相加, 再进行比较。
对于以上这几种方法,各有利弊,请细心选择。要想得到正确结果的前提是你要做出着色均匀、背景很浅的高质量 切片。
11)在什么情况下进行组织抗原修复, 抗原修复的条件是什么?
1 、由于组织中部分抗原在甲醛或多聚甲醛固定过程中,发生了蛋白之间交联及醛基的封闭作用,从而失去抗原性。 通过抗原修复,使得细胞内抗原决定族重新暴露,提高抗原检测率。
2 、修复方法从强到弱一般分为三种, 高压修复、微波修复、胰酶修复。修复液也分为若干种(具体的可以查阅相 关资料,大量的:中性的、高 pH 的等)。
3 、微波修复,一般用 6min*4 次,效果不错。
12) 内源性过氧化物酶的灭活时间和浓度是什么?
1、一般 3%过氧化氢灭活时间短点,可以 10min 左右;而 0.3%过氧化氢则可以适当延长封闭时间,一般 10~30min。
2 、用甲醇配置过氧化氢比双蒸水或 PBS 可能好在保护抗原和固定组织作用,过氧化氢孵育时间过长易引起脱片.
3 、现用现配,配好后 4 度避光保存。
13)如何才能充分脱蜡?
1 、蜡不溶于水, 如果脱蜡不干净,少许蜡存留于切片上,将会引起染色不均匀、阳性物时隐时现、真假难辨、背 景染色增加等。为了解决上述的问题,切片在染色前必须彻底脱蜡,目前用于脱蜡的试剂主要是二甲苯, 因它脱蜡
力强,脱蜡时间较短;
2 、脱蜡的时间要根据季节,室温和试剂的新鲜谋面是在不同。如果在夏天,室温较高,脱蜡试剂也新鲜, 则脱蜡 时间不需很多,3-5 分钟就已足够。如果在冬天, 室温较低, 脱蜡试剂也较陈旧,则脱蜡时间需要延长, 10-20 分钟 或更长。
3 、当天切的切片, 烧烤 2 小时后进行染色,切片带有温度进行脱蜡这将可加速脱蜡的过程,如果预先切好烤好的 切片,在染色前,还必须对切片进行加温 10-20 分钟,然后再行脱蜡, 这样脱蜡速度加快,效果魁伟更好。
总之,操作时应根据不同的季节,不同的室温,不同的试剂来决定,脱蜡的时间,原则上是要彻底、干净、完全地 脱去切片上的蜡。
14)如何最大限度地降低组织非特异性染色?
1 、缩短一抗/二抗孵育时间、稀释抗体来控制。这是最重要的一条。
2 、一抗用多克隆抗体易出现非特异性着色,建议试用单克隆抗体看看。
3 、内源性过氧化物酶和生物素在肝脏、肾脏等组织含量很高(含血细胞多的组织),需要通过延长灭活时间和增加 灭活剂浓度来降低背景染色;
4、非特异性组分与抗体结合,这需要通过延长二抗来源的动物免疫血清封闭时间和适当增加浓度来加强封闭效果;
5 、缩短 DAB 孵育时间或降低 DAB 浓度/过氧化氢浓度等;
6 、适当增加 PBS 冲洗次数和浸洗时间,在一抗、二抗或 SP 孵育之后的浸洗尤为重要;
7 、防止标本染色过程中出现干片,这容易增强非特异性着色。
15)背景染色较深的原因有哪些?
1、抗体浓度过高:一抗浓度过高是常见的原因之一。解决办法是,每次使用新抗体前应当对其工作浓度进行测试, 使每一抗体个体化,找到适合自己实验室的理想工作浓度, 既使是即用型的抗体也应如此,不能只简单的按说明书 进行染色。
2 、抗体孵育时间过长或温度较高:解决办法是, 严格执行操作规程, 最好随身佩带报时表或报时钟,及时提醒, 避免因遗忘而造成时间延长。现在流行的二步法(Polymer)敏感性很高,要求一抗孵育的时间不是传统的 1 小时, 而是 30 分钟,因此,要根据染色结果进行调整。
3、DAB 变质和显色时间太长:DAB 最好现用现配,如有沉渣应进行过滤后再用。配制好的 DAB 不应存放时间太长, 因为在没有酶的情况下,过氧化氢也会游离出氧原子与 DAB 产生反应而降低 DAB 的效力,未用完的 DAB 存放在冰 箱里几天后再用这种似乎节约的办法是不可取的。DAB 的显色最好在显微镜下监控,达到理想的染色程度时立即终 止反应。不过当染色片太多时或用染色机时, 这样做似乎不现实,但至少应对一些新的或少用的抗体显色时进行监 控,避免显色时间过长。
4 、组织变干:修复液溢出后未及时补充液体、染色切片太多、动作太慢、忘记滴液、滴液流失等都是造成组织变 干的原因。解决的办法是操作要认真仔细,采用 DAKO 笔或 PAP Pen 在组织周围画圈, 可以有效的避免液体流失, 也能提高操作速度。
5 、切片在缓冲液或修复液中浸泡时间太长(大于 24 小时):原因上不清楚, 但现象存在。有的实验室喜欢前一天 将切片脱蜡至修复,第二天加抗体进行免疫组化染色,如果将装有切片和修复液的容器放在 4ºC 冰箱过夜,对结果 无明显影响,如果放在室温, 特别是炎热的夏天,会出现背景着色,因此, 不可存放时间太长。
6 、一抗变质、质量差的多克隆抗体:注意抗体的有效期, 过期的抗体要么不显色要么背景着色。用新买抗体时最 好设立阳性对照和用使用过的抗体作比较。

科研服务咨询

公众号二维码