
概念:
凡是来源于胚胎、组织器官及外周血,经特殊分离方法制备而来的原初培养的细胞称之为原代细胞。原代细胞离体时间短且不经过永生化过程,其生物学特性未发生很大变化,仍保持原有的遗传特征,可更好地反映细胞在体内的生长状态,从而获得与体内生理功能更接近的数据,很适合用于药物测试、细胞分化和转化等实验研究。
原理介绍:
原代细胞的分离是将人/小鼠等特异模式动物的细胞从机体中取出,经胰酶、螯合剂(常用EDTA)处理,分散成单细胞,置合适的培养基中培养,使细胞得以生存、生长和繁殖的过程。 原代培养是指直接从机体取下细胞、组织和器官后立即进行培养。因此,较为严格地说是指成功传代之前的培养,此时的细胞保持原有细胞的基本性质,如果是正常细胞,仍然保留二倍体数。但实际上,通常把第一代至第十代以内的培养细胞统称为原代细胞培养。最常用的原代培养有组织块培养和分散细胞培养 。
实验方法:
一、悬浮细胞的分离方法
组织材料若来自血液、 羊水、胸水或腹水的悬液材料, 最简单的方法是采用 1000r/min 的低速离心 10 分钟,若悬液量大,可适当延长离心时间,但速度不能太高,延时也不能太长,以避免挤压或机械损伤细胞,离心沉淀用无钙、镁 PBS 洗两次,用培养基洗一次后,调整适当细胞浓度后再分瓶培养,若选用悬液中某些细胞,常采用离心后的细胞分层液,因为,经离心后由于各种细胞的比重不同可在分层液中形成不同层,这样可根据需要收获目的细胞。
二、实体组织材料的分离方法
对于实体组织材料,由于细胞间结合紧密,为了使组织中的细胞充分分散,形成细胞悬液,可采用机械分散法(物理裂解)和消化分离法。其中,机械分散法的特点是简便、快速,但对组织机械损伤大,而且细胞分散效果差,适用于处理纤维成分少的软组织。消化分离法是指把组织剪切成较小团块(或糊状),应用酶的生化作用和非酶的化学作用进一步使细胞间的桥连结构松动,使团块膨松,由块状变成絮状,此时再采用机械法,用吸管吹打分散或电磁搅拌或在摇珠瓶中振荡,使细胞团块得以较充分的分散,制成少量细胞群团和大量单个细胞的细胞悬液,接种培养后,细胞容易贴壁生长。
三、小鼠肝细胞原代培养
1、取肝脏:将小鼠断颈致死,取肝脏;
2、除杂物:剔除脂肪、结缔组织、血液等杂物;
3、研磨肝脏:用手术剪将脏器剪成小块并研磨;
4、胰酶消化:加入胰酶消化,使细胞分离;
5、滤网去杂:用滤网过滤,除去大组织块;
6、细胞计数:血球计数板计数。
原代培养注意事项:
(1)原代培养材料的选择,尽量选取繁殖能力较强的组织,如胚胎、幼小的生物体或者肿瘤组织等。
(2)样本必须为无菌采取完整的组织块,新鲜组织离体后置于无菌培养基中,冰袋运输。离体时间不可超过4小时。
(3)整个取材操作要迅速,尤其孕鼠浸泡乙醇时间1min左右,不能过长,以确保胚胎细胞活性。
(4)运用消化法时胰酶温度应低于37℃,浓度只需平时消化细胞浓度的一半。因为此过程不像消化培养细胞时的1~10min,而是至少20min,先消化下来的细胞在此胰酶消化液中继续消化了10min以上。所以胰酶不能作用过强,否则这些细胞易被损伤而不易生存。
(5)如使用组织块法,则应待组织块略干燥,能黏附于瓶壁时再使之与培养液接触,匆使组织块漂浮起来。如果组织块没有黏壁,则细胞不易生长,即使生长也因没有贴在瓶壁上,从而因不能观察到而无法收集到生长的细胞。
(6)原代培养操作时,也可以使用未添加血清的DMEM或PBS洗涤子宫、胚胎或组织块等。
(7)本实验也可以使用新生乳鼠做培养材料。此时要将乳鼠浸入75%乙醇2~3min使皮肤充分消毒,由于乳鼠原代培养污染概率更高,故应小心操作,避免污染细菌。乳鼠原代培养细胞的存活率不及胚胎细胞培养的成功率。
案例展示:
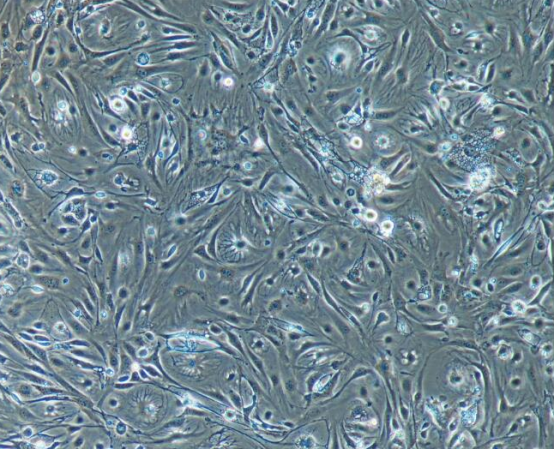
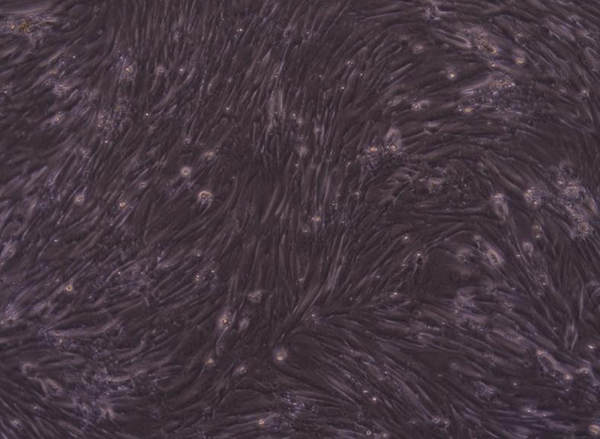

科研服务咨询

公众号二维码