IF:8.1,丝滑思路再升级!这套高分组合思路能够轻松实现转换与复现!
题目:二甲双胍通过调节FoxO1核胞浆穿梭改善HPRT1靶向嘌呤代谢并修复NR4A1介导的自噬治疗绝经后骨质疏松症
英文名:Metformin improves HPRT1-targeted purine metabolism and repairs NR4A1-mediated autophagic flux by modulating FoxO1 nucleocytoplasmic shuttling to treat postmenopausal osteoporosis
杂志:Cell Death & Disease
影响因子:8.1/Q1
发表时间:2024年11月
研究背景:骨质疏松症是一种主要的退行性代谢性骨病,威胁着绝经后妇女的生命和健康。由于检测方法和预防策略意识的局限性,骨质疏松症治疗的目的更多的是延缓进一步恶化,而不是从根本上纠正骨量。本研究旨在阐明绝经后骨质疏松症的发病机制并优化治疗方案。
研究思路:实验基于先前的发现,即氧化应激介导雌激素缺乏后骨代谢失衡。通过能量代谢靶向代谢组学,揭示了嘌呤代谢紊乱是诱导骨组织氧化损伤的主要机制,这通过使用来自人类数据库的机器学习数据得到了验证。黄嘌呤和黄嘌呤氧化酶用于治疗成骨细胞,构建嘌呤代谢紊乱模型。X/XO处理后成骨细胞活性和分化能力下降。转录组测序表明,自噬通量损伤与嘌呤代谢诱导的成骨细胞氧化应激有关。此外,进行血清代谢组学结合网络药理学,以确定二甲双胍治疗绝经后骨质疏松症的药理机制。HPRT1是从枢纽基因过滤的潜在靶标,FoxO1信号传导是介导二甲双胍在成骨细胞中作用的关键途径。还揭示了SIRT3介导的脱乙酰化促进了FoxO1的核定位,从而增加了HPRT1的表达。HPRT1上调促进嘌呤合成代谢,阻止嘌呤分解代谢引起的ROS积累,以逆转成骨细胞的氧化损伤。

研究结果:
1、骨能量代谢靶向代谢组学和机器学习
对假手术组和卵巢切除组样本进行能量代谢靶向代谢组检测(图1A,B)。随后进行重复相关分析(图1C),最小偏二乘判别分析(OPLS-DA)(图1D),筛选出31种有效差异丰富代谢物(图1E-G),生成差异丰富代谢物的热图(图1H)。如图1I,J所示,嘌呤代谢在这两组之间存在显著差异。嘌呤相关代谢物在OVX组中积累。发现KKNN和SVM模型在预测骨质疏松方面表现出突出的性能,这从框图中每个模型的平均AUC中可以明显看出(图1K,L),KKNN模型的验证结果通过接收器工作特征(ROC)曲线分析进一步突出了其outstanding性,曲线下面积(AUC)值为0.875(图1M)。这些结果表明嘌呤代谢相关基因对于区分绝经后骨质疏松症患者和健康对照具有很高的诊断价值。

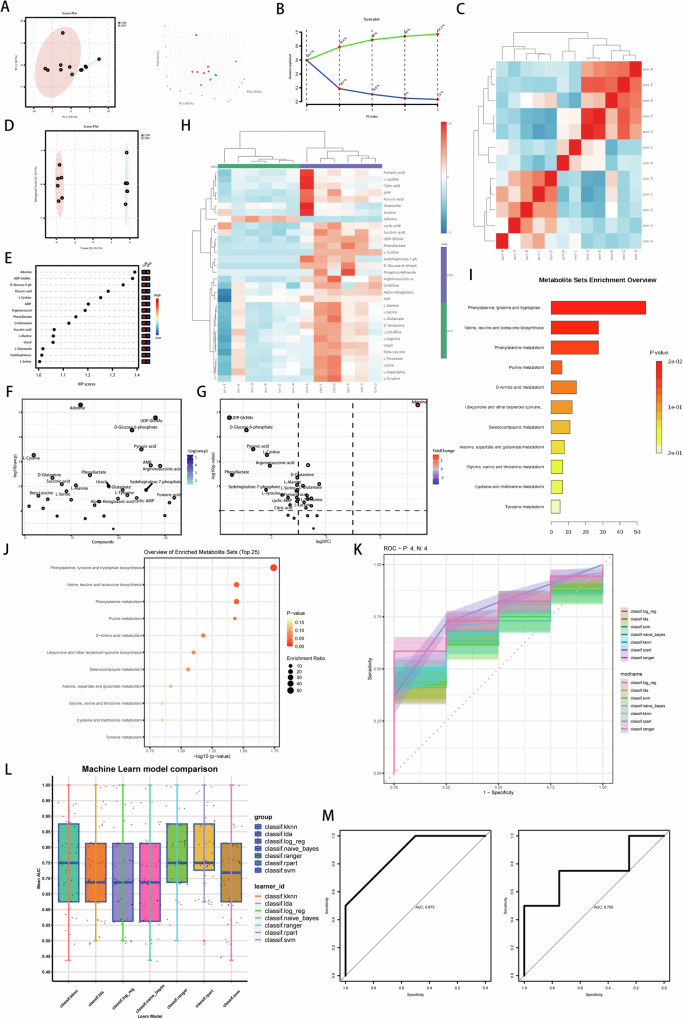
图1
2、代谢组学和网络药理学的综合分析
micro-CT结果表明二甲双胍可以防止骨丢失并改善OVX小鼠的骨显微结构(图2A)。进行了血清代谢组学分析,以确定OVX组和二甲双胍实验组之间差异丰富的代谢物(图2B,)。这两组样品之间的差异通过多模态PCA可视化(图2C)。所有差异丰富的代谢物根据其内容在图2D中列出。此外,进行了网络药理学分析,获得了1871个骨质疏松相关靶点和47个二甲双胍相关靶点(图2E)。从分子功能(MF)、生物过程(BP)和细胞成分(CC)三个方面分析基因功能,并确定了前十大术语(图2G)。GO分析后,根据MF分析共鉴定出5个功能组(图2H-I)。KEGG网络如图2J所示。通过将网络药理学分析揭示了HPRT1和CANT1是上述枢纽基因,受影响的途径是嘌呤代谢(图2K)。
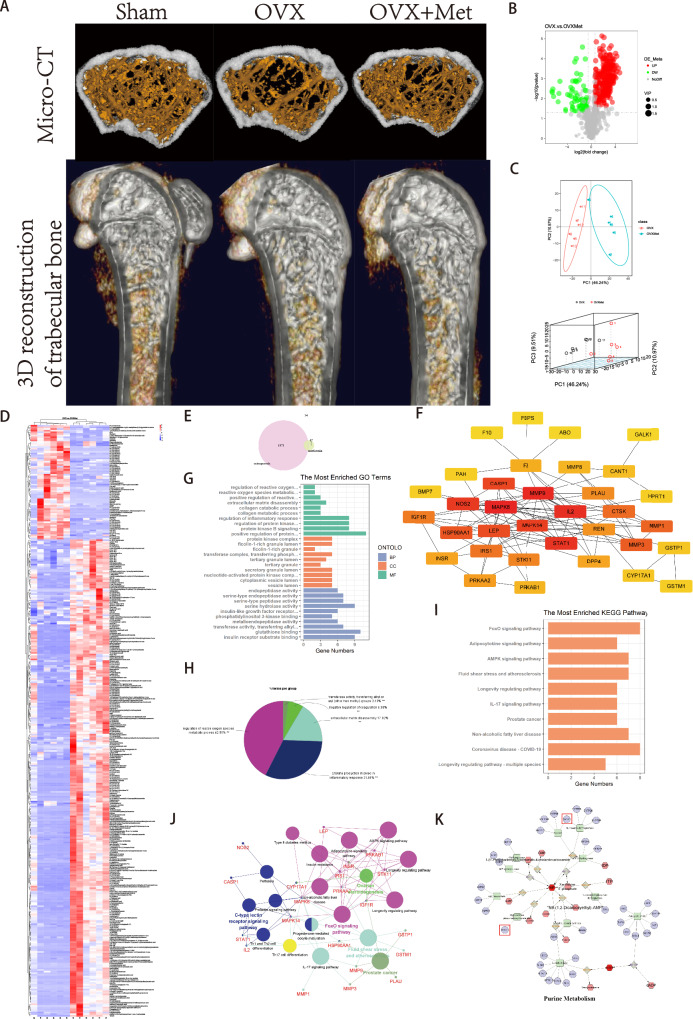
图2
3、二甲双胍减轻X/XO诱导的成骨细胞损伤
通过CCK-8和流式细胞仪测定(图3A,B)确定具有足够黄嘌呤浓度(100µmol)用于分解的黄嘌呤氧化酶的the best浓度(图3A,B)。结果显示,25mU/ml黄嘌呤氧化酶显着降低了生存能力,同时增加了凋亡成骨细胞的百分比(图3A,C)。因此,25mU/ml黄嘌呤氧化酶用于后续实验。随后探索了二甲双胍在治疗绝经后骨质疏松症中的作用。实验显示,200mmol二甲双胍显着逆转了X/XO治疗引起的细胞生存能力和凋亡细胞百分比的下降(图3D-F)。因此,200mmol二甲双胍用于后续实验。
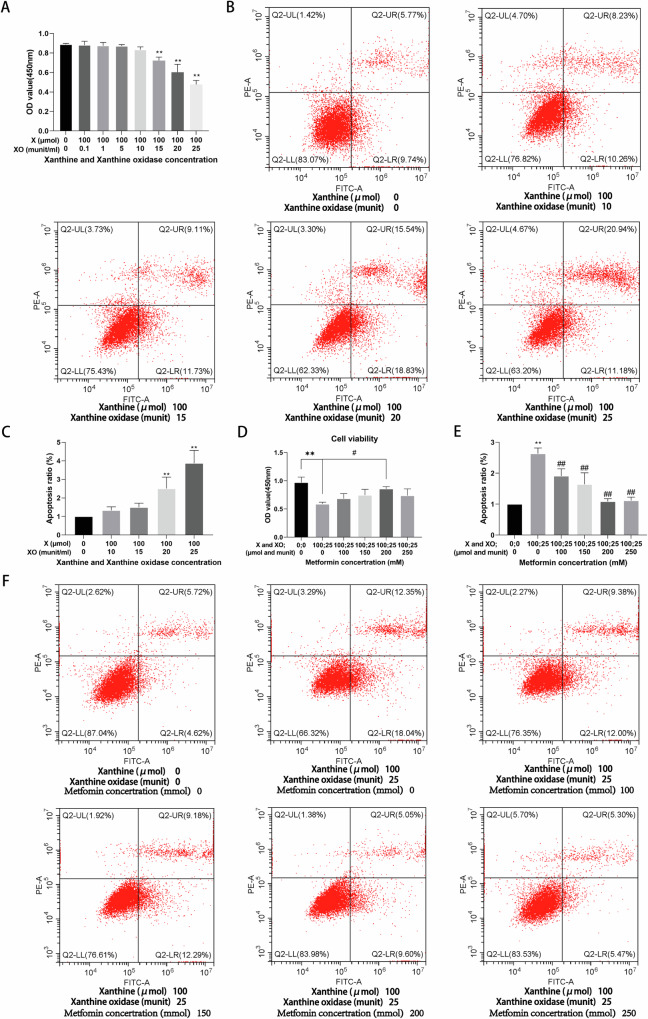
图3
4、二甲双胍增加HPRT1表达以逆转成骨细胞的氧化损伤
对股骨组织样本进行免疫组织化学分析,以确认HPRT1在体内表达的变化(图4A)。HPRT1的表达随着二甲双胍体外干预而增加(图4B,C)。HPRT1表达抑制后凋亡细胞的百分比增加(图4D,E)。二甲双胍增加了相关蛋白的比例,这在HPRT1沉默后被逆转(图4B,C)。如图4F所示,二甲双胍在X/XO处理后恢复了成骨细胞的分化和矿化能力。沉默HPRT1表达逆转了二甲双胍的治疗效果,结果表明,线粒体膜电位随着X/XO处理而降低,ROS水平增加,二甲双胍的治疗效果通过沉默HPRT1而逆转(图4G,H,I)。细胞内钙离子浓度也显示了氧化损伤的程度(图4J)。这些结果表明二甲双胍上调HPRT1的表达,以改善成骨细胞中X/XO诱导的氧化应激损伤。
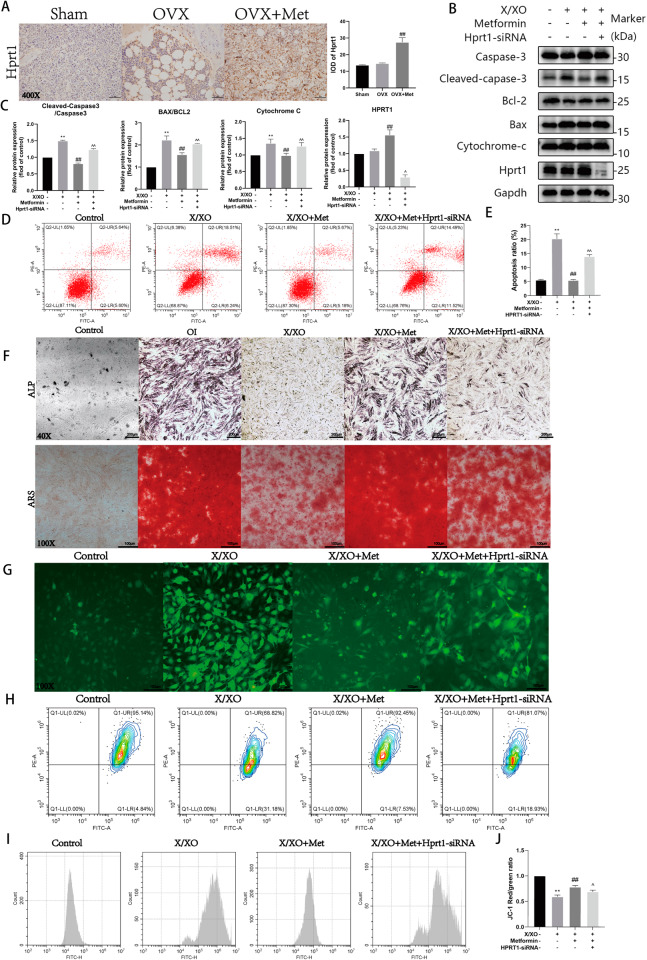

图4
5、SIRT3介导的FoxO1脱乙酰化促进其核定位以调节HPRT1表达
OVX和二甲双胍治疗组的FoxO1水平低于假手术组(图5a)。在细胞水平,添加As184来抑制FoxO1表达,HPRT1蛋白水平下降(图5B,C)。Sirt3基因沉默逆转了这些影响,并降低了相应HPRT1蛋白的水平(图5D-G)。二甲双胍处理增加了FoxO1蛋白定位于核的比例,但Sirt3沉默逆转了这种影响(图5H)。与野生型细胞相比,K245R转染细胞中FoxO1的核定位增加,相应地,HPRT1蛋白水平升高(图5I,J,L)。K245R组显示更多的FoxO1蛋白核定位,而K245Q组显示相反(图5K)。这些发现表明SIRT3对FoxO1的调控是通过位点-245的乙酰化实现的。
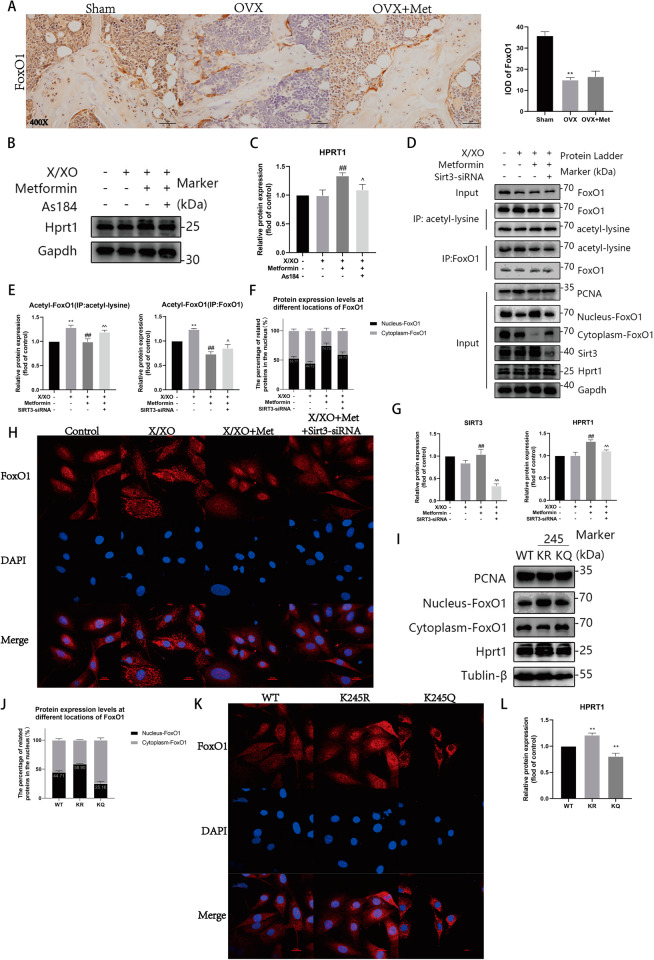

图5
6、转录组数据表明,自噬与X/XO诱导的氧化损伤有关
与对照组相比,X/XO组共鉴定出2028个上调基因和2184个下调基因(图6A和S1D)。GO分析表明,DEG富集在“利用自噬机制的加工”、“自噬”、“溶酶体膜”、“溶酶体”、“溶解液泡”和“自噬体”(图6B,C)中。KEGG分析还显示了溶酶体和自噬相关通路的富集(图6D-F)。此外,将这些参数的变化与二甲双胍治疗后观察到的变化进行了比较。结果显示二甲双胍治疗后248个上调基因和301个下调基因(图6G)。GO分析还揭示了二甲双胍可以调节嘌呤核糖核苷和氧化还原辅酶代谢(图6H,I)。KEGG分析揭示富集在FoxO信号通路和自噬相关通路中的基因与上述发现一致(图6J,K)。为了鉴定X/XO和二甲双胍都参与自噬调控的因素,构建了DEGs的维恩图(图6L),根据基因的差异对其进行排序,并选出前15个基因进行进一步筛选。
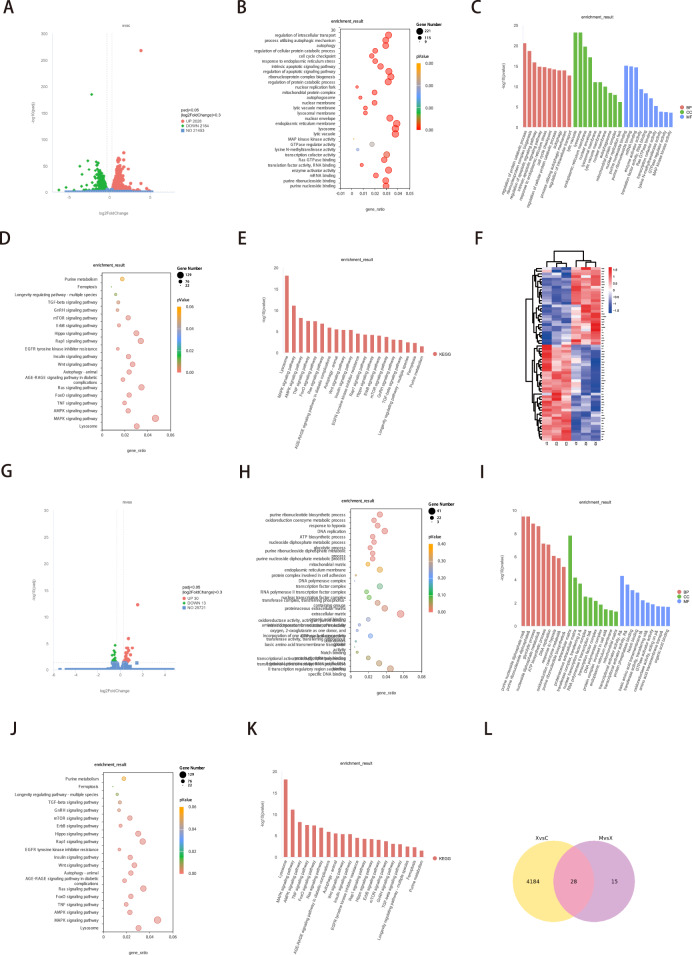

图6
7、自噬通量受损介导X/XO诱导的成骨细胞氧化损伤
使用透射电镜验证自噬和溶酶体的变化,二甲双胍大大增加了自溶酶体的数量,减少了自噬体的数量(图7A)。两种自噬标志物的表达在OVX组比假手术组更大,但在二甲双胍实验组更低,这与转录组分析的结果一致(图7B)。然后,使用Western blotting检测p62和LC3BII/I的蛋白质表达水平,这表明在X/XO处理后有所增加(图7C,D)。此外,检测了成骨细胞活性对CQ处理的响应。结果显示,二甲双胍对细胞凋亡和分化的治疗作用被CQ逆转(图7E,F,G)。与二甲双胍治疗相比,CQ添加增加了细胞内ROS水平,降低了X/XO环境中的线粒体膜电位(图7H,I)。细胞内钙浓度的增加也表明响应CQ治疗的氧化损伤程度增加(图7J)。此外,成骨细胞被mRFP-GFP-LC3腺病毒感染,以准确观察和评估自噬的变化。X/XO组的结果表明黄点(自噬体)比例增加,红点(自溶酶体)比例减少,这表明自噬通量被阻断。二甲双胍减弱了斑点比例的变化,但在CQ治疗后逆转(图7K,L)。这些结果表明自噬通量受损对于X/XO诱导的成骨细胞氧化损伤至关重要。
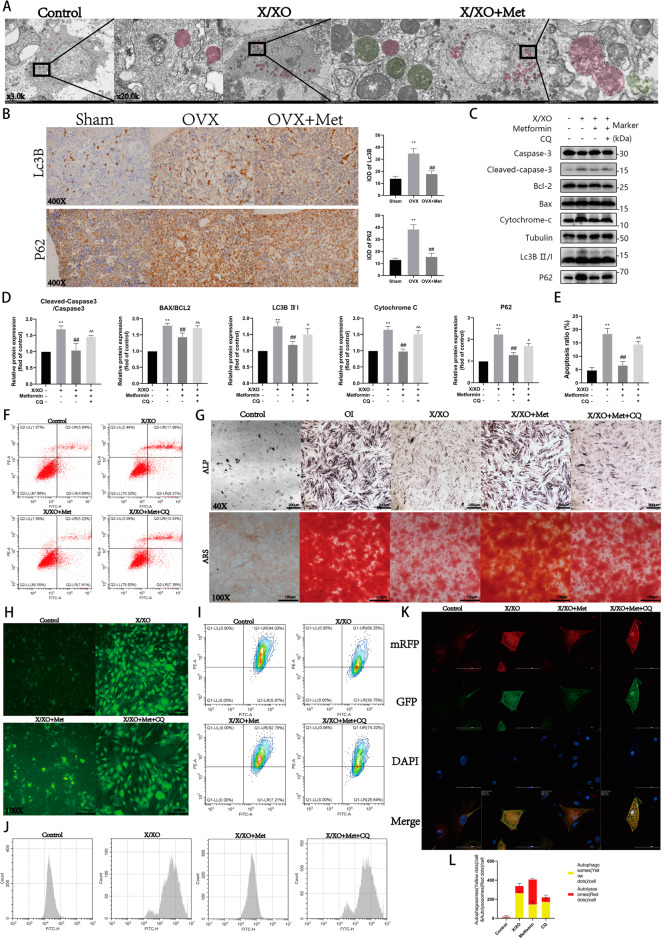
图7
8、二甲双胍通过恢复Nr4a1介导的自噬通量来改善X/XO诱导的氧化损伤
为了确定Nr4a1在调节自噬中的作用,首先进行免疫组织化学分析以确定骨组织中的Nr4a1含量(图8A)。随后通过添加Nr4a1-siRNA生成Nr4a1沉默的细胞以进一步验证。Western blotting显示(图8B,C)。如图8D,E所示,通过沉默Nr4a1基因,黄点(自噬体)与红点(自溶酶体)比例的变化被逆转。Western blotting结果表明,Nr4a1蛋白的表达水平随着X/XO处理而降低,HPRT1沉默后二甲双胍的治疗效果被逆转(图8F)。最后,构建HPRT1-overexpressing和Nr4a1沉默的细胞,以评估HPRT1是否可以通过Nr4a1进一步调节自噬通量。与X/XO组相比,HPRT1-overexpressing组LC3BII/I和p62的表达降低,Nr4a1基因的沉默逆转了这些影响(图8G,H)。自噬通量测试结果显示,HPRT1过表达后黄点(自噬体)比例下降,红点(自溶酶体)比例增加,这种影响通过沉默Nr4a1基因而逆转(图8I,J)。
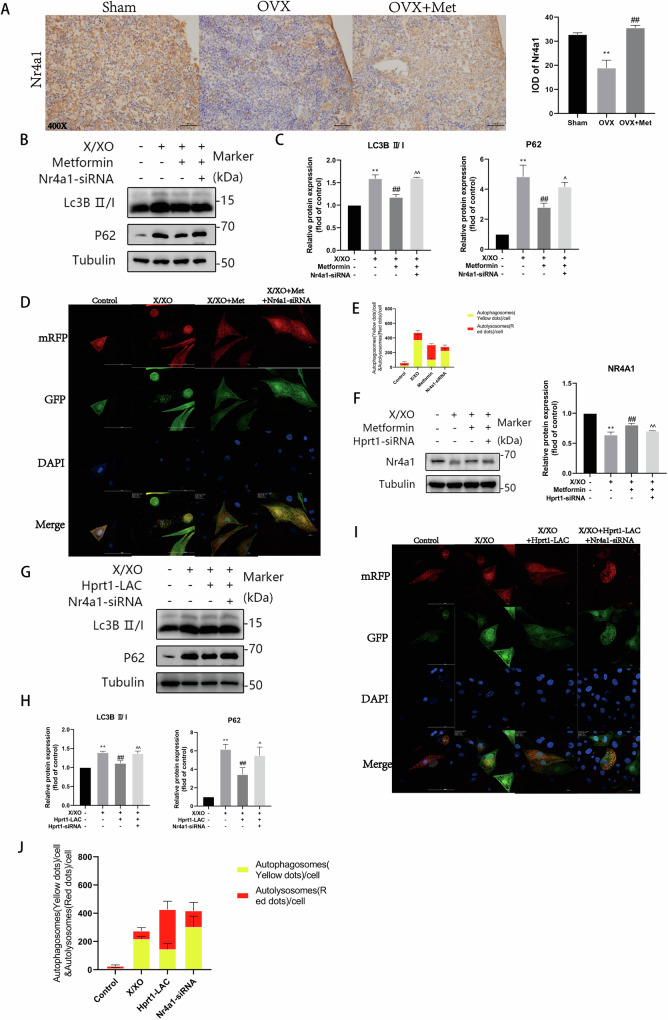
图8
总结:本文采用“代谢组学+转录组+机器学习+网络药理学+细胞自噬”深度挖疾病机制的神级思路,想不发一区都难!文章方法易复现,傲星生物不仅具有丰富的分析经验、还提供完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




