网络药理学+分子对接,开发双疾病药食同源药物,并实验解析了机制!
题目:抗焦虑和抗抑郁药物-食品类似物的网络药理学筛选、体外和体内评估
英文名:Network pharmacology screening, in vitro and in vivo evaluation of antianxiety and antidepressant drug-food analogue
杂志:Phytomedicine
影响因子:6.7/Q1
发表时间:2024年9月
研究背景:抑郁症和焦虑症是常见的精神疾病,而目前使用的化学药物通常会产生严重的不良反应。中国拥有丰富的药食两用中草药,以其安全有效而著称。本研究旨在利用网络药理学等技术,从药用和食用草本植物中开发出具有更好抗抑郁和抗焦虑效果的新型制剂,并在体外和体内实验中验证其效果。
研究思路:利用网络药理学和分子对接,确定具有抗焦虑和抗抑郁潜力的药材。进一步筛选出具有细胞保护作用和无毒特性的草药,配制成草药混合物。随后,建立PC12细胞损伤模型和小鼠慢性不可预测轻度应激(CUMS)模型,以评估配方的效果。结果初步筛选了十种药材,其中六种适合配制混合物,即甘草、大枣、钩藤、桑叶、黄芪和金银花(GDGSHJ)。GDGSHJ配方可减少乳酸脱氢酶(LDH)的渗漏,减少细胞凋亡,并在CUMS小鼠模型中显示出良好的抗抑郁和抗焦虑作用。此外,GDGSHJ还能上调血清中5-羟色胺(5-HT)的含量和脑组织中5-HT、γ-氨基丁酸(GABA)和多巴胺(DA)的水平。它还下调了小鼠海马中SLC6A4和SLC6A3基因的表达,同时上调了HTR1A、DRD1、DRD2和GABRA1基因的表达。该制剂具有强大的抗抑郁和抗焦虑作用,且不会产生严重毒性,这种功效似乎是由小鼠海马内相关基因的表达介导的,通过平衡血清中的5-HT水平和脑组织中的DA、GABA和5-HT水平来达到这一效果。
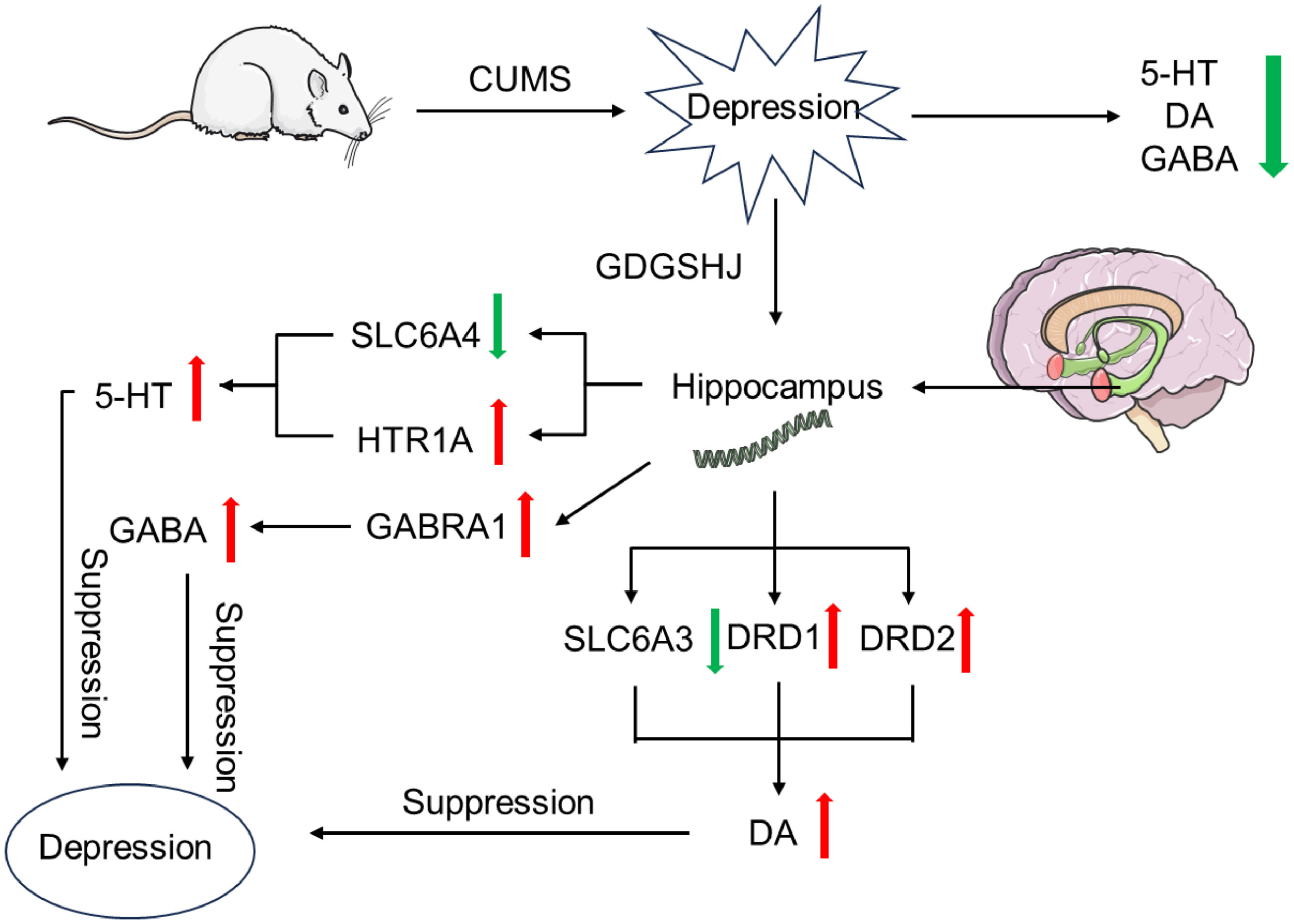
图1
研究结果:
1、网络药理学分析结果
通过数据库搜索共确定了103个交叉靶标(图2A),构建了一个PPI网络(图2B)。其中,度值在22或以上的49个节点被认定为本研究的核心靶点。随后生成了"焦虑和抑郁靶点-活性成分-同源草药"网络(图2C)。在49个靶标中,有26个可以与120种活性成分负匹配,相当于来自同一来源的79种草药。采用直接拓扑分析计算中药材节点及其相应活性成分的度值之和,确定边缘的数量。选取边值maximum的前10种药材,包括甘草、桑叶等,进行进一步研究(图2D)。
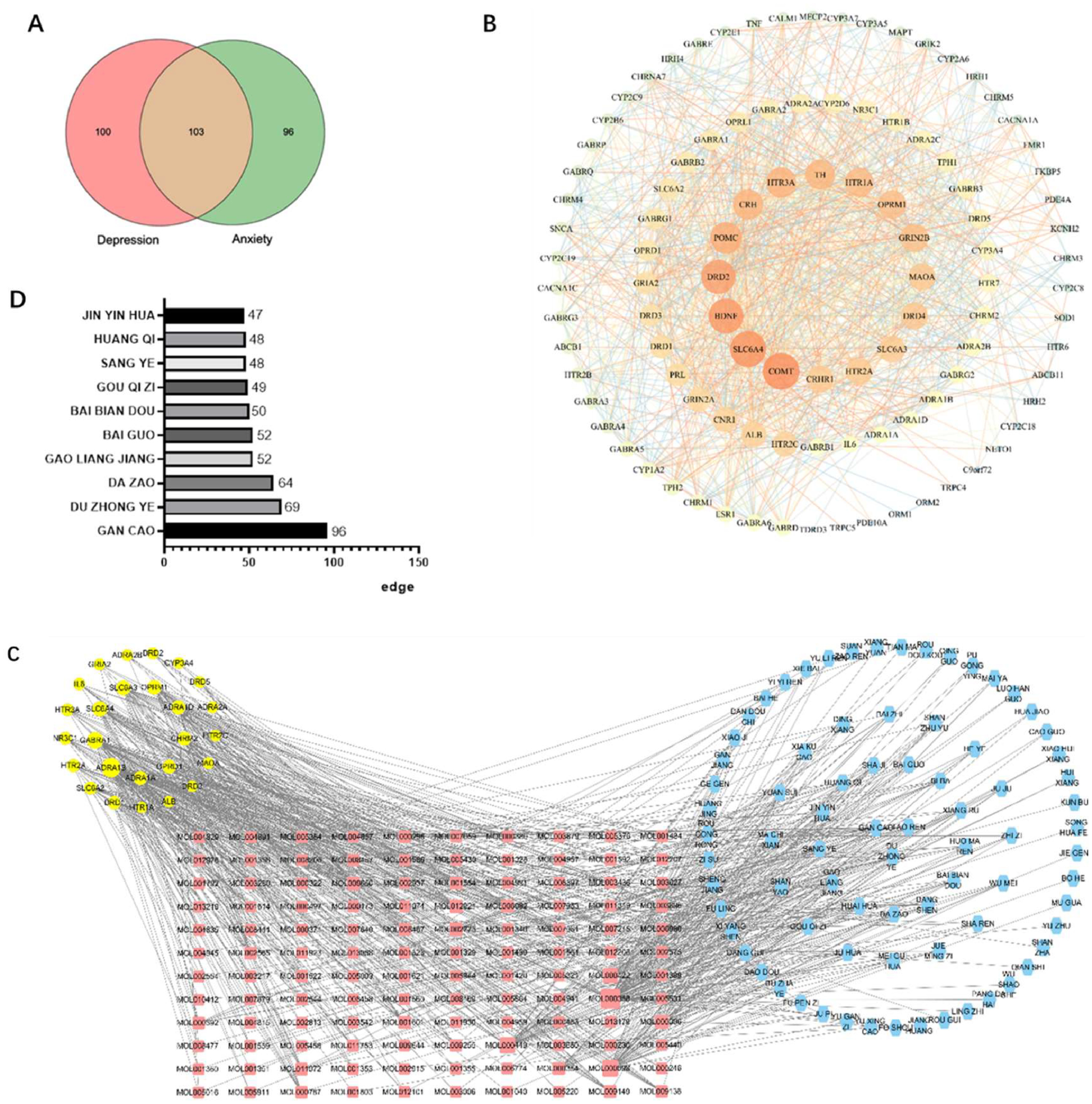

图2
从子网络中提取的十种核心药材被用于构建"核心药材-有效成分-抑郁和焦虑靶点"网络(图3A)。根据富集基因的数量,前十名结果以柱状图显示(图3B)。这些靶标主要与G蛋白偶联受体信号通路和化学突触传递等生物过程有关。在细胞组成方面,它们与细胞质膜组成等方面有关。分子功能则与蛋白质结合、G蛋白偶联受体活性等有关。KEGG富集分析共发现了9条通路,包括神经活性配体-受体相互作用和钙信号通路(图3C)。

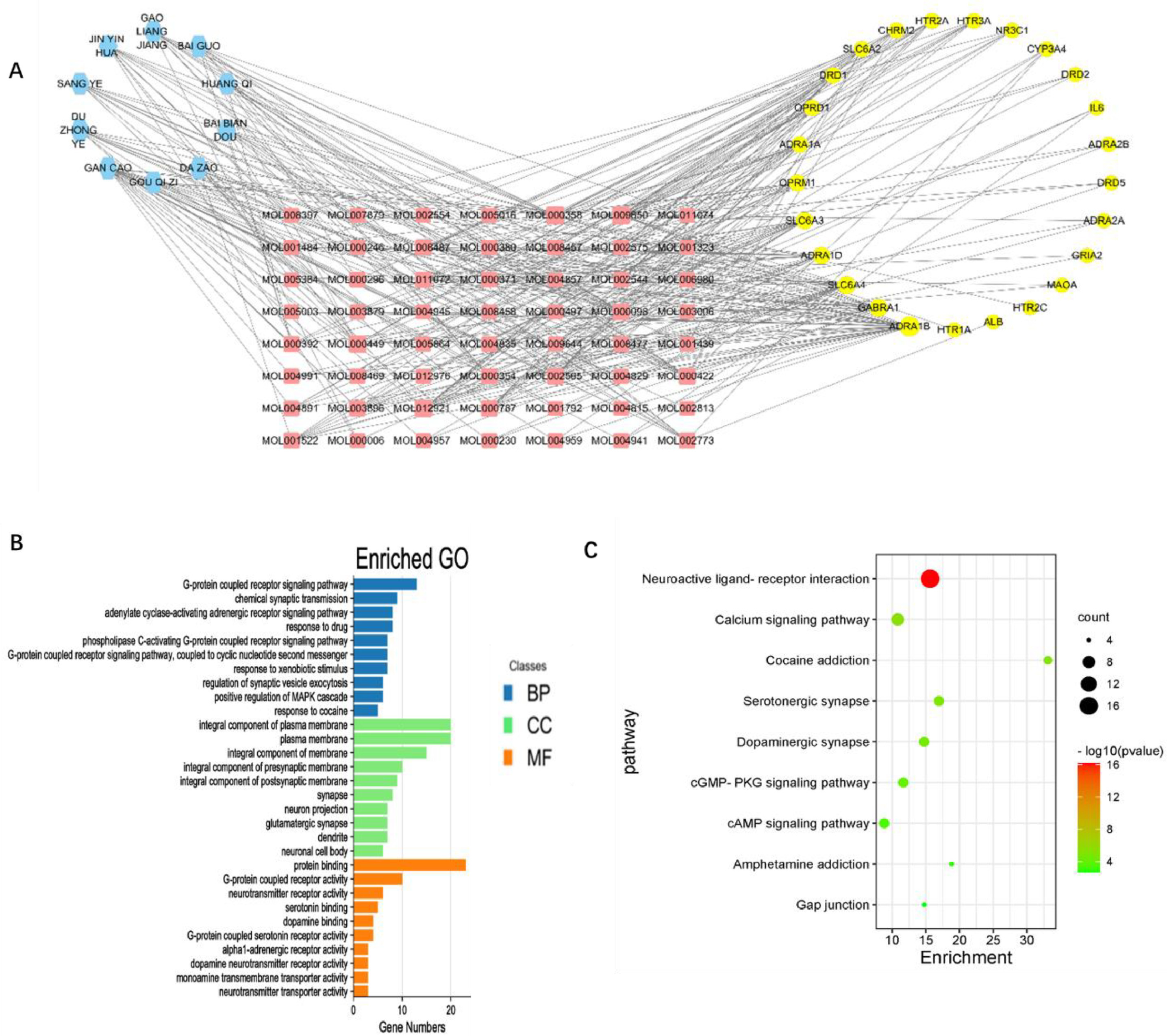
图3
2、分子对接结果
在"核心药用植物-活性成分-抑郁和焦虑靶标"网络中,以25个靶标作为受体蛋白,以主要的7种核心成分作为配体,进行了175次分子对接。一般来说,较小的结合能表明配体与受体之间的结合活性更强。在25个抑郁和焦虑靶点中,大多数都表现出与关键活性成分的良好结合活性(图4A)。其中,β-谷甾醇与HTR2C的结合活性highest,结合能为-10.7 kcal/mol,其次是豆甾醇与DRD2和美迪卡品与SLC6A4。三维图形显示了与目标结合活性the best的活性成分的对接模式(图4B)。
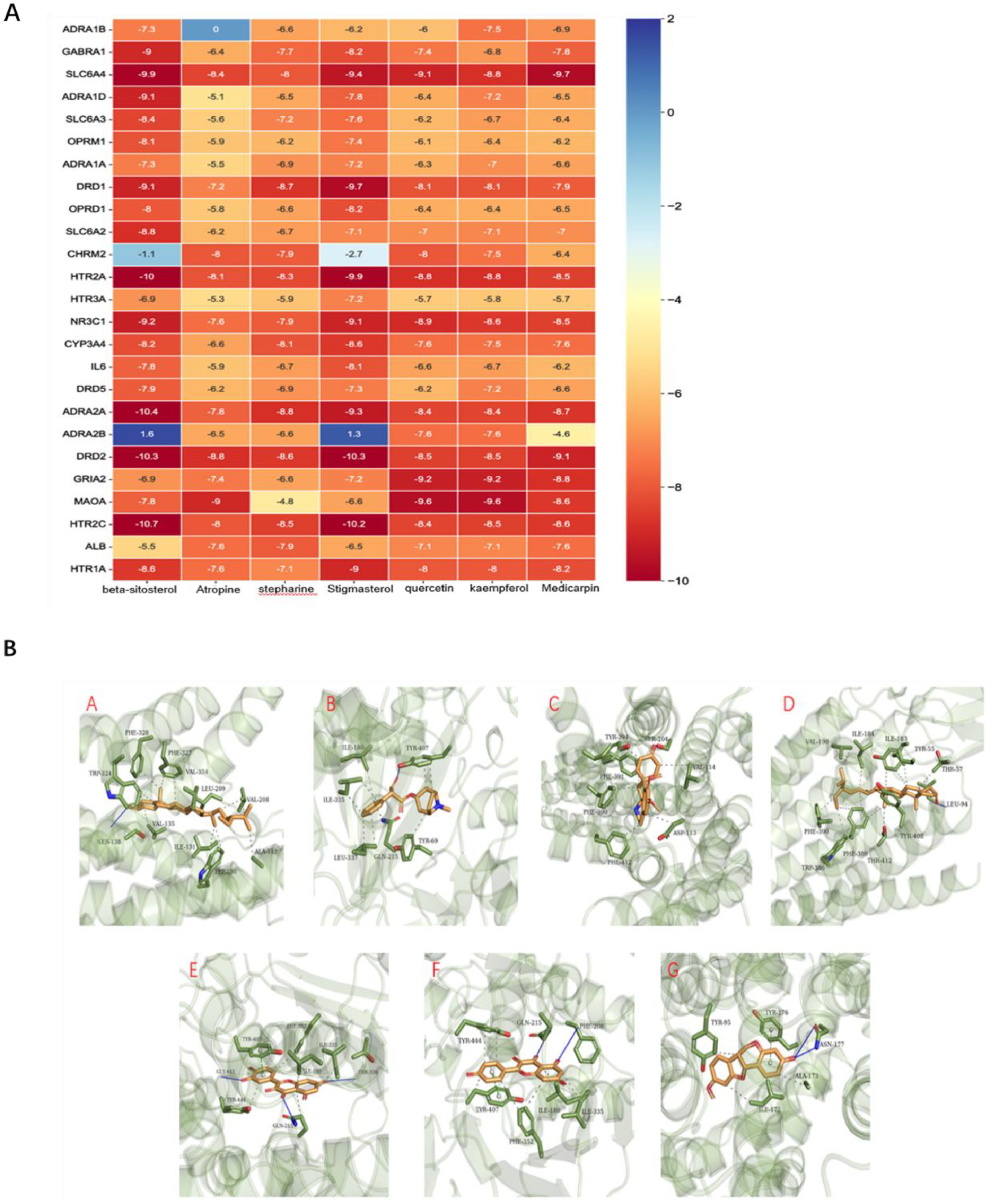
图4
3、GDGSHJ制剂对皮质酮处理的PC12细胞的保护作用
将400μM浓度的皮质酮暴露于PC12细胞24小时后,PC12细胞的增殖率下降了50.80±3.69%,表明细胞受到了严重破坏(图5)。在研究10草药对皮质酮诱导的PC12细胞增值率的影响(图6)。100mg/L甘草干预后的PC12细胞活性为63.93±7.6%。值得注意的是,400mg/L大灶、勾七子、桑烨、黄骐和金银化的干预导致PC12细胞活性分别为72.38±7.04%、65.23±2.48%、72.11±4.63%、75.51±4.67%和75.46±1.73%。相反,独中叶(200和400mg/L)、高梁江(200和400mg/L)和百果(400mg/L)对皮质酮诱导的PC12细胞表现出毒性作用。白编豆在0-400mg/L浓度范围内,对皮质酮处理的PC12细胞无显著影响。在50、100、200和400mg/L的浓度下,GDGSHJ制剂有效逆转细胞损伤,降低LDH活性,改善皮质酮诱导的PC12细胞膜损伤,并以剂量依赖性方式抑制皮质酮诱导的细胞凋亡(图7)。

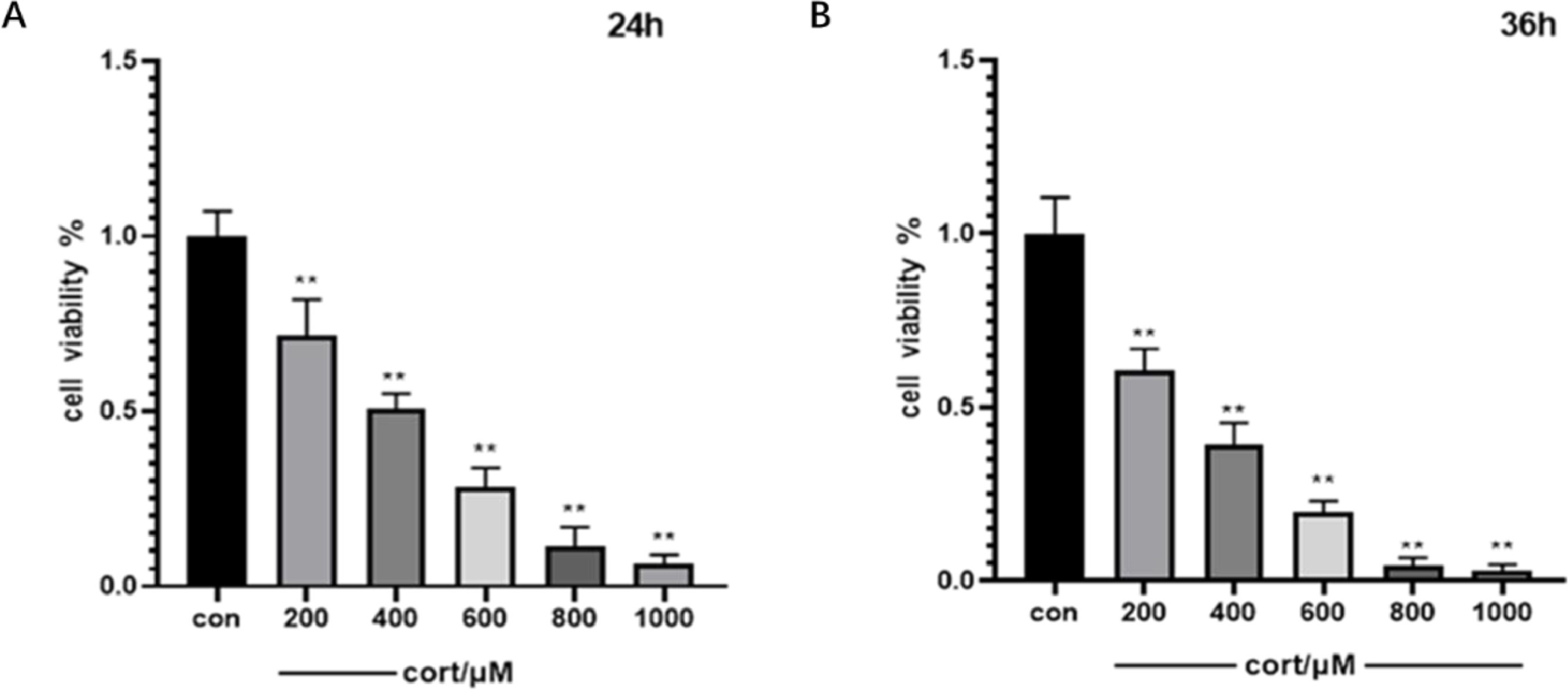
图5

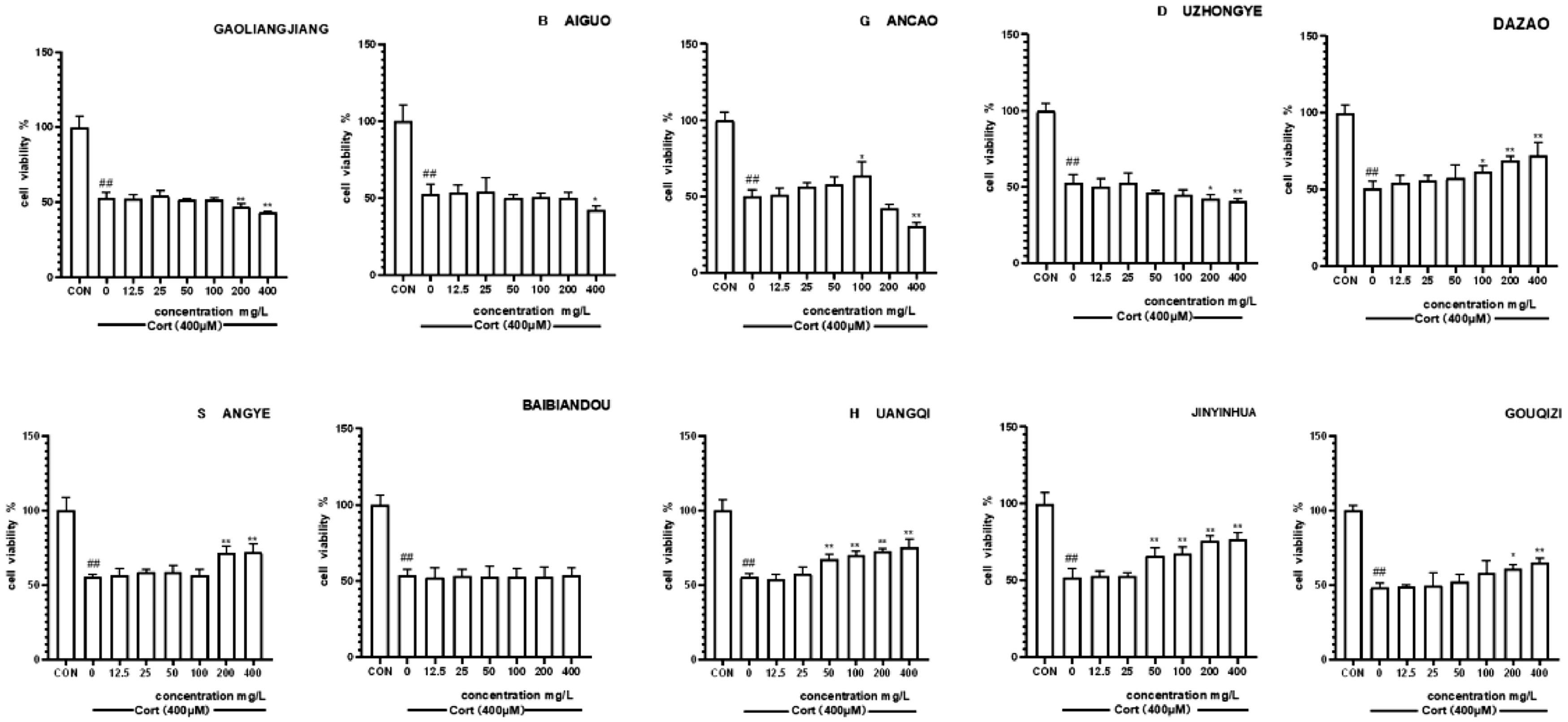
图6
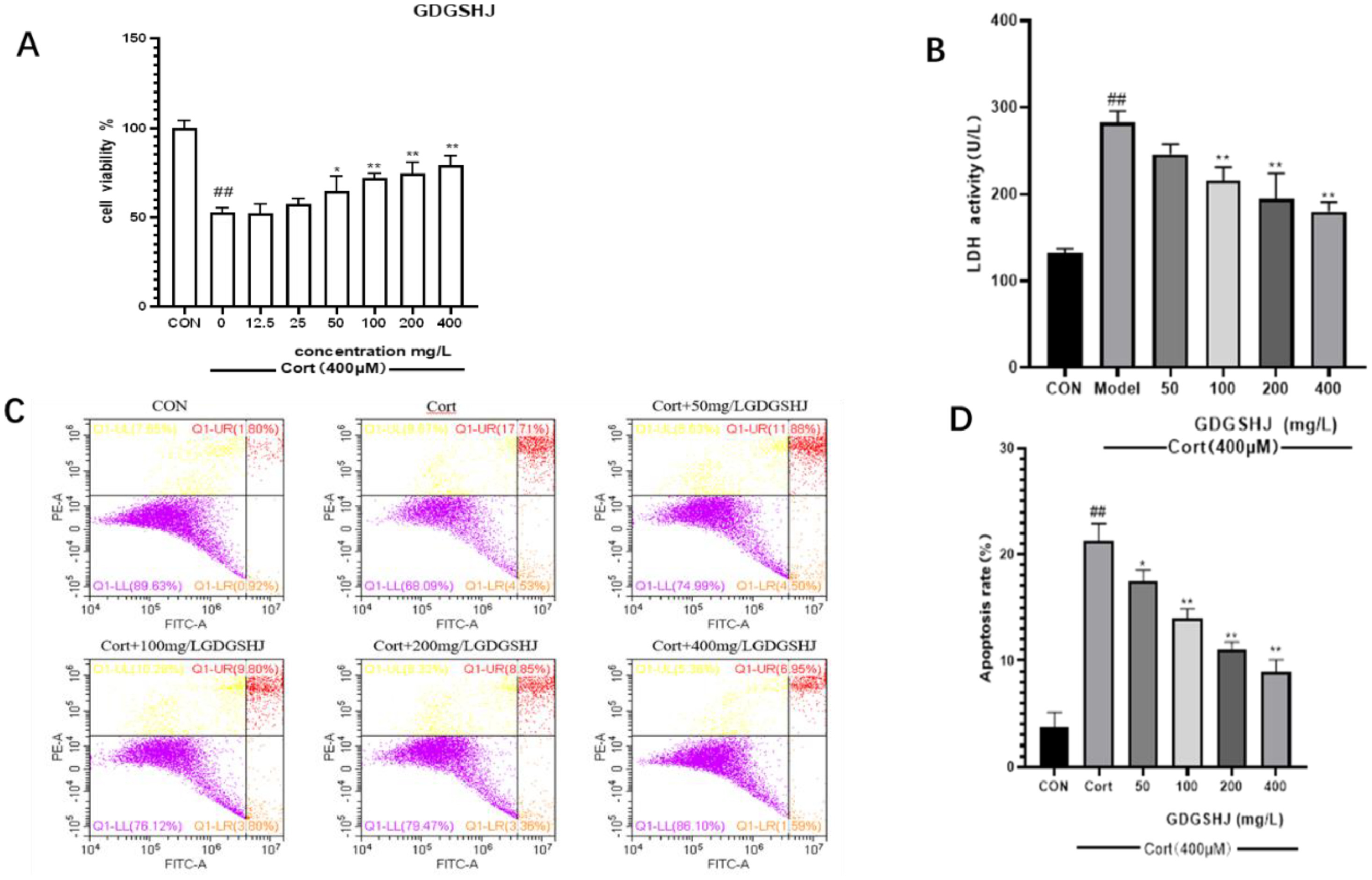

图7
4、GDGSHJ制剂缓解小鼠的焦虑抑郁样行为
模型制作完成后,模型组小鼠的体重增加明显低于正常组,同时还出现了毛发凌乱。这些症状在中剂量GDGSHJ和文拉法辛组明显逆转。在糖水偏好实验中,模型组小鼠的糖水偏好率(42.04±7.72%)明显低于空白组(84.59±4.36%)。开阔地实验表明,与空白组(25064±4539mm,29.03±12.05s)相比,模型组小鼠在中心区的总行进距离和停留时间(11830±6011mm,6.31±3.57s)均有所减少。EPM结果显示,模型组的焦虑指数(86.80±6.44%)高于正常组(52.39±8.26%)。与正常对照组(82.6±10.57s,66.9±10.49s)相比,模型组的FST和TST显示固定时间延长(135.6±10.76s,115.4±9.43s),表明建模成功。GDGSHJ中剂量组和高剂量组明显逆转了这些情况,表明其具有很强的抗抑郁活性(图8)。
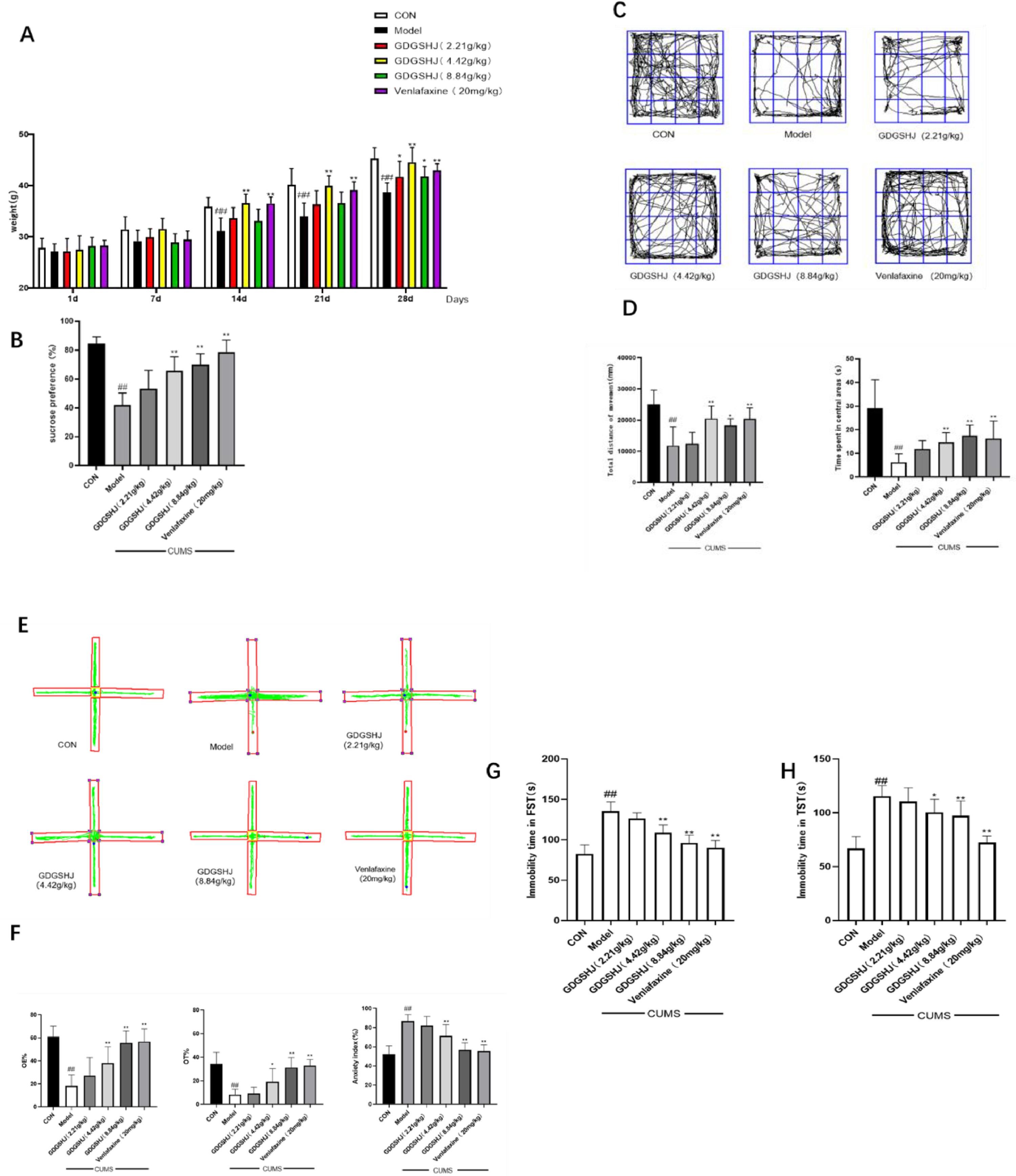
图8
5、GDGSHJ制剂可增加小鼠血清和脑组织中神经递质的水平
在小鼠神经递质水平方面,空白组的血清中5-HT和NE水平分别为185.75±11.83ng/mL和378.32±32.64pg/mL。CUMS刺激模型组的血清5-羟色胺(150.85±6.38ng/mL)和NE(294.84±20.01pg/mL)水平显著下降。阳性对照药物文拉法辛明显提高了血清5-HT和NE的水平。同时,中、高剂量的GDGSHJ对血清5-HT水平有明显调节作用,但对NE水平无明显影响。虽然有明显的趋势,但CUMS小鼠的血清GABA和DA与空白对照组没有明显差异(图9)。在脑组织中,空白组的5-HT、NE、GABA和DA水平分别为195.39±12.88ng/mL、372.03±36.08pg/mL、301.06±21.92pg/mL和301.06±21.92。pg/mL和168.45±12.70pg/mL。模型组在接受CUMS刺激后,5-HT(160.64±8.27ng/mL)、NE(301.26±32.57pg/mL)、GABA(228.34±7.53pg/mL)和DA(134.43±6.30pg/mL)明显下降。使用阳性药物文拉法辛可逆转这些效应,导致脑组织中的5-羟色胺、GABA和DA含量增加。同样,与CUMS组相比,中剂量和高剂量GDGSHJ均能显著提高脑组织中5-羟色胺、GABA和DA的含量。然而,GDGSHJ对脑组织中NE的影响不明显(图10)。

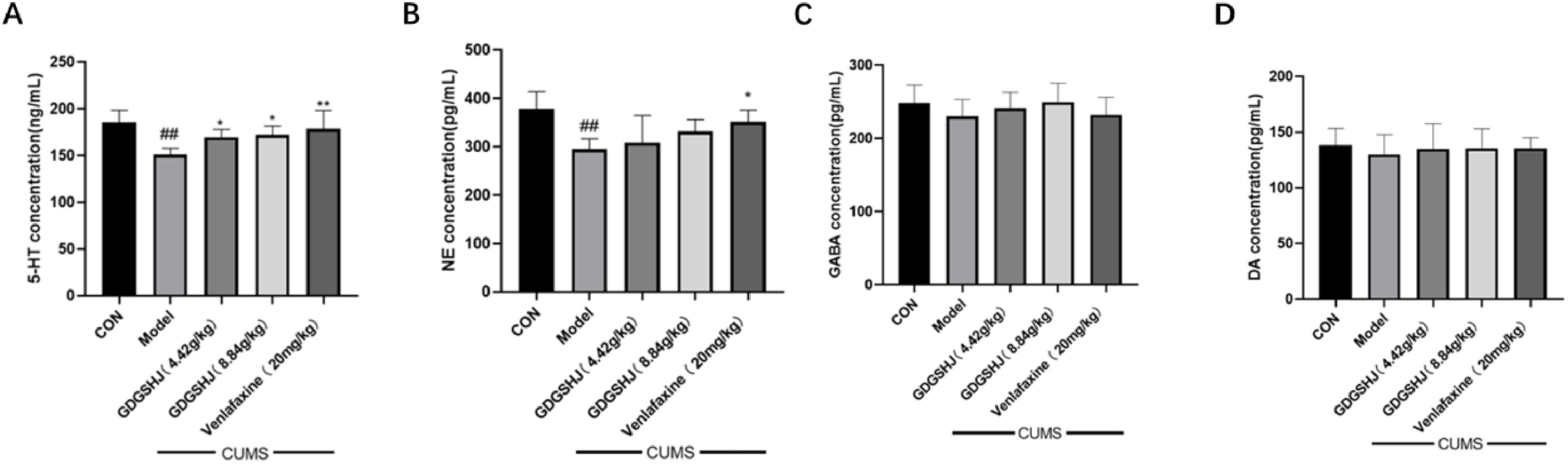
图9
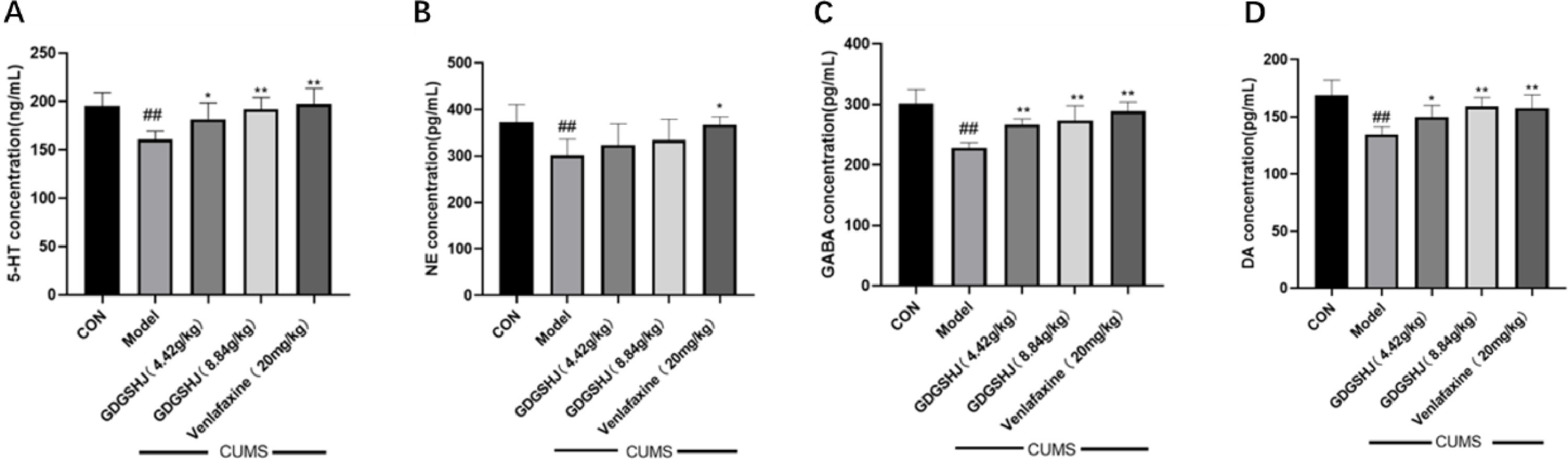 图10
图10
6、GDGSHJ制剂影响CUMS小鼠海马部分预测靶基因的mRNA表达
在CUMS刺激后,小鼠海马区SLC6A4和SLC6A3基因的mRNA表达明显上调。相反,HTR1A、DRD1、DRD2和GABRA1基因的mRNA表达则明显下调。相反,与模型组相比,给予中等剂量的GDGSHJ能显著逆转这些结果(图11)。
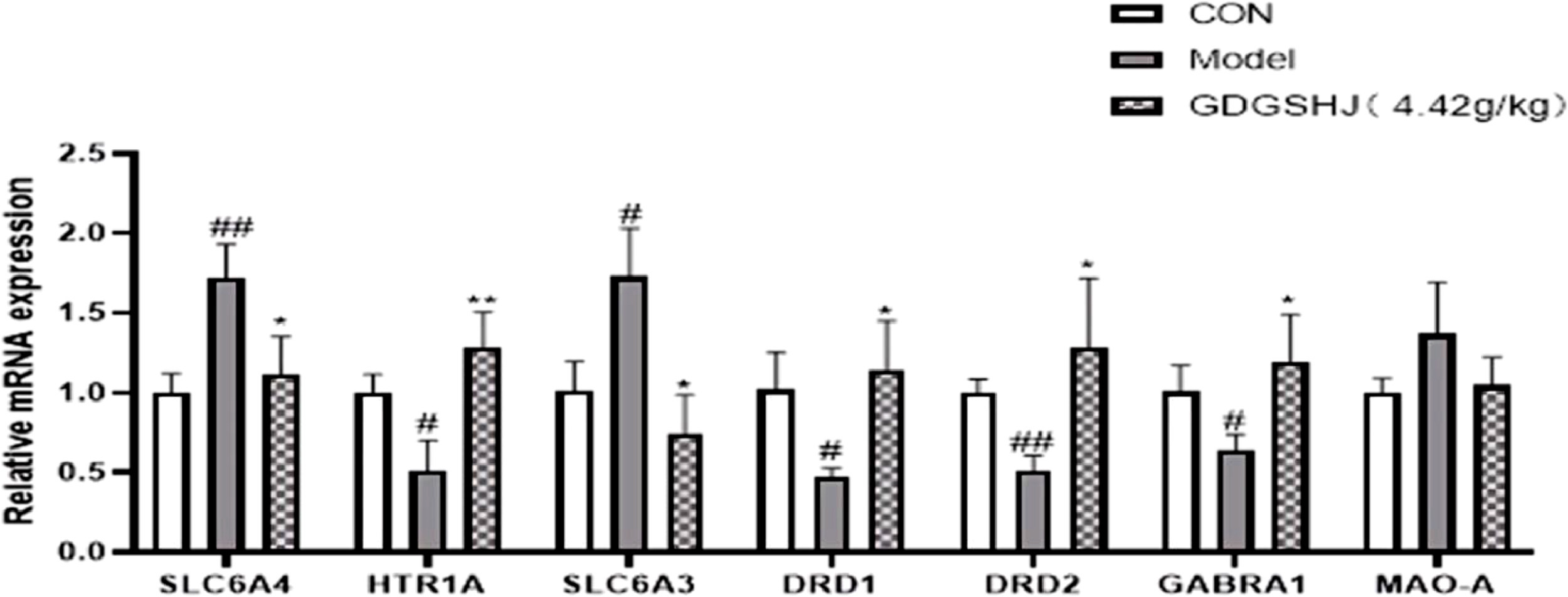
图11
总结:本文利用网络药理学的方法推出双疾病靶点有作用的中药配方,并且在体外做的验证,思路值得学习,文章中的分析方法还可以更丰富,傲星生物有丰富的分析方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




